
 A��B��C��D��E��FΪԪ�����ڱ�ǰ������Ԫ����ԭ��������������A�Ļ�̬ԭ����3����ͬ���ܼ������ܼ��е�������ȣ�B2-��C-��D+��E3+������ͬ�ĵ��ӹ��ͣ�DԪ�ص���ɫ��Ӧ�ʻ�ɫ��F�Ļ�̬ԭ�ӵļ۵����Ų�ʽΪ3d64s2��
A��B��C��D��E��FΪԪ�����ڱ�ǰ������Ԫ����ԭ��������������A�Ļ�̬ԭ����3����ͬ���ܼ������ܼ��е�������ȣ�B2-��C-��D+��E3+������ͬ�ĵ��ӹ��ͣ�DԪ�ص���ɫ��Ӧ�ʻ�ɫ��F�Ļ�̬ԭ�ӵļ۵����Ų�ʽΪ3d64s2��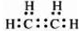 ��
������ A�Ļ�̬ԭ����3����ͬ���ܼ������ܼ��е�������ȣ���A�ĵ����Ų�ʽΪ1s22s22p2����AΪCԪ�أ�
DԪ�ص���ɫ��Ӧ�ʻ�ɫ����DΪNaԪ��
B2-��C-��D+��E3+������ͬ�ĵ��ӹ��ͣ�B��C��D��EΪԪ�����ڱ�ǰ������Ԫ����ԭ��������������BΪOԪ�أ�CΪFԪ�أ�EΪAlԪ�أ�
F�Ļ�̬ԭ�ӵļ۵����Ų�ʽΪ3d64s2����FΪFeԪ�أ�
��1��D2AB3ΪNa2CO3���������ӻ������Ӧ�л��ƻ����Ӽ���D3EC6ΪNa3AlF 6 ��AlF 6-�������ӣ�Al������ԭ�ӣ�F-Ϊ��λ�壻
��2��CO2�ǷǼ��Է��ӣ�����ԭ��C�Ĺ���ӻ���ʽΪsp�����ӹ�����ֱ���ͣ�CO2����ԭ���γɵ�һ���⻯���к���5���Ҽ���1���м������⻯��Ϊ��ϩ��
��3�����ڵ�����Ԫ����F��O��F�ĵ縺�Խϴǽ�����ǿ��F 2 �ɽ�ˮ�е����û�����������O�ҷ��ӹ����ǡ�V���͵ķ�����H 2O��SO 2��O 3�ȣ�
��4�����ݾ����и�ԭ����Ŀ�жϻ�ѧʽ�����ݺϽ��ܶ�$��=\frac{m}{V}$��
��� �⣺A�Ļ�̬ԭ����3����ͬ���ܼ������ܼ��е�������ȣ���A�ĵ����Ų�ʽΪ1s22s22p2����AΪCԪ�أ�
DԪ�ص���ɫ��Ӧ�ʻ�ɫ����DΪNaԪ��
B2-��C-��D+��E3+������ͬ�ĵ��ӹ��ͣ�B��C��D��EΪԪ�����ڱ�ǰ������Ԫ����ԭ��������������BΪOԪ�أ�CΪFԪ�أ�EΪAlԪ�أ�
F�Ļ�̬ԭ�ӵļ۵����Ų�ʽΪ3d64s2����FΪFeԪ�أ�
��1��D2AB3ΪNa2CO3���������ӻ������Ӧ�л��ƻ����Ӽ���Na3AlF 6 ��AlF 6-�������ӣ�Al������ԭ�ӣ�F-Ϊ��λ�壬
�ʴ�Ϊ�����Ӽ���F-��
��2��CO2�ǷǼ��Է��ӣ�����ԭ��C�Ĺ���ӻ���ʽΪsp�����ӹ�����ֱ���ͣ�CO2����ԭ���γɵ�һ���⻯���к���5���Ҽ���1���м������⻯��ΪCH2=CH2�������ʽΪ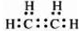 ��
��
�ʴ�Ϊ��sp��ֱ���Σ�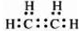 ��
��
��3�����ڵ�����Ԫ����F��O��F�ĵ縺�Խϴǽ�����ǿ��F 2 �ɽ�ˮ�е����û�����������O�ҷ��ӹ����ǡ�V���͵ķ�����H 2O��SO 2��O 3�ȣ�
�ʴ�Ϊ��F��O��O3��SO 2��
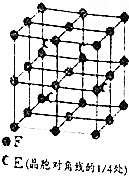
��4�������к�����ԭ�Ӹ���Ϊ$8��\frac{1}{8}+6��\frac{1}{2}+12��\frac{1}{4}+1=8$������Alԭ��Ϊ4����˻�ѧʽΪFe2Al����þ������ܶ�Ϊ�ѣ����Цѡ���a��10-7�� 3��N A=4����56��2+27�������=$\frac{5.56��1{0}^{23}}{{a}^{3}{N}_{A}}$��
�ʴ�Ϊ��Fe2Al��$\frac{5.56��1{0}^{23}}{{a}^{3}{N}_{A}}$��
���� �����Ƕ����ʽṹ�����ʵĿ��飬�漰�������͡���ѧ�������ӿռ乹�͡��縺�ԡ���������ȣ��Ƕ����ʽṹ����֪ʶ���ۺ��Կ��飬���Ƚϻ�����ע��������������ʵ�Ӱ�죮


 ������״Ԫ���Ծ�ϵ�д�
������״Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Һ��ʱ����ˮӦ�������ܵ��϶˽��룬�¶�����������ˮ���ʹ���ԭ�� | |
| B�� | ����ʱ����������������ֽ��һ�߽Ӵ���©���¶˽����ձ��ڱ� | |
| C�� | ������������ʱ��������ȫ������ʱ��ֹͣ���� | |
| D�� | ��Һʱ�������÷ֲ��������ʹ�²�Һ�����������²�Һ�պ������������ر��������ٻ���һֻ�ձ����ٴ����������ϲ�Һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ʹ����Ӧ�����ʷ�����Ӧ | |
| B�� | �����ڻ�ѧ��Ӧǰ��ѧ���ʺ����������� | |
| C�� | �����ܸı仯ѧ��Ӧ���� | |
| D�� | �κλ�ѧ��Ӧ������Ҫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH+HCl�TNaCl+H2O | B�� | 2Fe3++Fe�T3Fe2+ | ||
| C�� | Zn+2HCl�TZnCl2+H2�� | D�� | 4Al+3O2+6H2O�T4Al��OH��3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮʱ��ƽ�����淴Ӧ�����ƶ� | |
| B�� | ���������������ƹ��壬��Һ��c��OH-����С | |
| C�� | ͨ������HCl���壬ƽ��������Ӧ�����ƶ� | |
| D�� | ��������NH4Cl���壬ƽ��������Ӧ�����ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
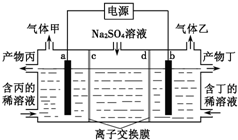
| A�� | a�����Դ�ĸ������� | |
| B�� | �����Ϊ������Һ | |
| C�� | ���ӽ���ĤdΪ�����ӽ���Ĥ | |
| D�� | ÿת��0.1mol e-�����1.12L������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
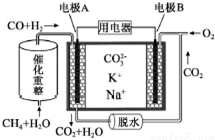
| A�� | �缫A��H2����ĵ缫��ӦΪ��CO+H2+2CO32--4e-=3CO2+H2O | |
| B�� | �����ϣ�A��ÿ����1molH2��������$\frac{1}{3}$molCH4 | |
| C�� | ��ع���ʱ��CO32-��缫A�ƶ� | |
| D�� | �缫B�Ϸ����ĵ缫��ӦΪ��O2+2CO2+4e-=2CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com