
【题目】科学家从某中草药提取的有机物结构如下图所示。下列说法正确的是

A. 分子式为C14H10O6
B. 环上氢原子被取代,所得一氯代物有3种
C. 1mol该有机物与足量NaOH溶液反应最多消耗4mol NaOH
D. 该有机物的熔点可能比同碳原子的烃分子熔点高
 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
①1L0.1mol/LNH4NO3溶液中氮原子数小于0.2NA
②用标准盐酸滴定NaOH 溶液测其浓度时,酸式滴定管用蒸馏水洗涤后,没用标准盐酸润洗,直接装标准盐酸滴定,所测的碱液浓度偏低
③PH相等的四种溶液: a.CH3COONa b.C6H5ONa c.NaHCO3 d.NaOH。(已知酸性:C6H5OH2CO3),其溶液物质的量浓度由小到大顺序为:d、b、c、a
④钢铁腐蚀时可能发生的正极反应: 2H2O+O2+4e-=4OH-
⑤电解饱和MgCl2溶液时,电解反应式为:2H2O+2Cl-![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
⑥在海轮外壳连接锌块保护外壳不受腐蚀是采用牺牲阳极的阴极保护法
⑦长期使用硫酸铵,土壤酸性增强:草木灰与铵态氮肥不能混合施用
A. ①②⑤⑥ B. ①③⑤⑦ C. ②③④⑤ D. ③④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氮及其化合物的说法正确的是
A.N2化学性质稳定,可用作保护气
B.NO、NO2均为大气污染气体,在大气中可稳定存在
C.NO、NO2均易溶于水
D.NO、NO2均能与水发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表除去括号内杂质所用的试剂和方法都正确的是( )
选项 | 物质 | 所用试剂 | 方法 |
A | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
B | 乙醇(水) | 生石灰 | 分液 |
C | 乙醇(乙酸) | 氢氧化钠溶液 | 分液 |
D | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于浓HNO3与浓H2SO4的叙述正确的是( )
A.常温下遇铁都发生钝化B.常温下都能与铜反应产生氢气
C.露置于空气中,溶液质量均不变D.露置于空气中,溶液浓度均不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:

(1)电极X的材料是 (化学式);电解质溶液Y是 ;
(2)银电极为电池的 极,发生的电极反应为 ;X电极上发生的电极反应为 ;
(3)外电路中的电子是从 电极流向 电极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对某滴有酚酞的饱和NaCl溶液在如图装置中进行电解,回答下列问题:
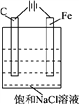
(1)C极现象为___________,Fe极(含其周围的溶液)现象为:_____________________。
(2)若电解一段时间以后,将电源反接,C极电极反应式为:___________________,溶液中可以观察到的现象是:_____________________________________________。再向该溶液中通入O2,又会观察到的现象是:________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
科学家研制出合成药物W对肝癌的治疗,具有很好的效果。其由有机物A合成药物W的合成路线如下:

已知:2HCHO+NaOH→CH3OH+HCOONa
②![]() (Diels-Aider反应)
(Diels-Aider反应)
③丁烯二酸酐结构简式为![]()
④当每个1,3-丁二烯分子与一分子氯气发生加成反应时,有两种产物:
CH2ClCH=CHCH2Cl;CH2ClCHClCH=CH2。
请回答下列问题:
(1)物质A中的含氧官能团名称为_______;第①步反应中除生成 外,还生成另一产物,此产物的结构简式为__________________。
外,还生成另一产物,此产物的结构简式为__________________。
(2)写出H的结构简式____________________;第⑤步反应的反应类型是____________________。
(3)药物W与N互为同分异构体。同时满足下列条件的N的同分异构体(不考虑立体异构)有__种。
①能与FeCl3溶液发生显色反应 ②能与Na2CO3溶液反应生成气体
③1mol N能与3mol NaOH完全反应
写出满足上述条件且其核磁共振氢谱有4个吸收峰的N的一种结构简式_____________________。
(4)下面是合成X的路线图:

则X的结构简式为___________________。
(5)结合题中有关信息,写出由![]() 制备丁烯二酸酐
制备丁烯二酸酐![]() 的合成路线流程图______________(无机试剂任选)。合成路线流程图示例如下:
的合成路线流程图______________(无机试剂任选)。合成路线流程图示例如下:

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铬(Cr)的本意是颜色,因为它的化合物或离子都有美丽的颜色。下表是几种常见含铬的离子水溶液的颜色:
离子 | Cr2O72- | Cr(OH)4 | Cr3+ | CrO42- | Cr2+ |
颜色 | 橙色 | 绿色 | 蓝紫色 | 黄色 | 蓝色 |
(1)铬铁矿的主要成分是Fe(CrO2)2,该物质中三种元素的化合价均为整数,则Cr的化合价是_____________。
(2)向Na2CrO4溶液中加入浓盐酸,溶液会变为蓝紫色并有黄绿色气体产生,则氧化剂和还原剂的物质的量之比为_____________。
(3)向Na2Cr2O7溶液中加入浓NaOH溶液,会变成黄色,请解释原因(用离子方程式和必要的文字说明)_____________________________________________。
(4)工业上以铬铁矿[主要成分为Fe(CrO2)2,含有Al2O3、Fe2O3、SiO2等杂质]为主要原料,生产重铬酸钠晶体(Na2Cr2O7·2H2O)。主要工艺流程如下:

①滤渣的成分是_____________(写化学式)
②写出煅烧过程中,所发生的非氧化还原反应的化学方程式(任写一个)______________________。
③煅烧过程中,所发生的氧化还原反应如下:(其中浸出液显黄色),请完成下面化学方程式并配平。
□Fe(CrO2)2+□Na2CO3+□O2=□_________+□Fe2O3+□CO2
④工业上在重铬酸钠溶液中加入适量稀硫酸,用石墨作电极电解生产金属铬,阴极的电极反应式为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com