
| 元素编号 | 元素性质与原子(或分子)结构 |
| X | 地壳中含量最高的非金属元素 |
| Y | M层比K层多1个电子 |
| Z | 最外层电子数为内层电子数的0.6倍 |
| W | 与氯形成的氯化物是生活中常用的调味品 |
分析 X为地壳中含量最高的非金属元素,为O元素,Y的M层比K层多1个电子,为Al元素,Z的最外层电子数为内层电子数的0.6倍,为S元素,W与氯形成的氯化物是生活中常用的调味品,为Na元素,结合对应单质、化合物的性质以及题目要求解答该题.
解答 解:X为地壳中含量最高的非金属元素,为O元素,Y的M层比K层多1个电子,为Al元素,Z的最外层电子数为内层电子数的0.6倍,为S元素,W与氯形成的氯化物是生活中常用的调味品,为Na元素,
(1)X为O,对应的双原子分子的结构式为O=O,对应的水中含有氢键,较一般的分子间作用力强,沸点较高,故答案为:O=O;最高;水分子间存在氢键;
(2)Y为Al,工业用电解熔融的氧化铝冶炼,方程式为2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑,故答案为:2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑;
(3)Al单质与Na元素的最高价氧化物对应水化物恰好反应完全,生成NaAlO2,向反应后的溶液中通入过量的CO2,生成氢氧化铝和碳酸氢钠,发生反应的离子方程式为AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-,故答案为:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-;
(4)1mol单质Zn与 2mol Z元素形成的强酸浓溶液反应生成硫酸锌和二氧化硫气体,可用品红检验,如品红褪色,且加热溶液变红,
故答案为:SO2;用品红检验,如品红褪色,且加热溶液变红;
(5)单质Na与有机物CH3CH(OH)COOH反应的化学方程式为2Na+CH3CH(OH)COOH→CH3CH(ONa)COONa+H2↑,
故答案为:2Na+CH3CH(OH)COOH→CH3CH(ONa)COONa+H2↑.
点评 本题考查了元素位置、结构和性质的关系,正确推断元素是解本题关键,结合元素在周期表中的位置、元素周期律来分析解答,注意相关化学方程式以及离子方程式的书写,难度中等.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 回收废旧电池,主要目的是回收其中的贵金属 | |
| B. | 减少石油使用,改用风能、太阳能、燃煤等能源,符合绿色化学的理念 | |
| C. | 在食品袋中放入盛有硅胶的透气小袋,可防止食物氧化变质 | |
| D. | 用浸泡过高锰酸钾溶液的硅藻土吸收水果中的乙烯,可以实现水果保鲜的目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
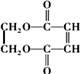 的合成路线如图:
的合成路线如图: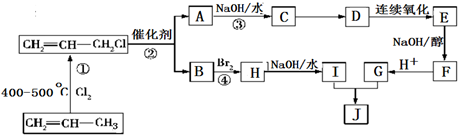
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
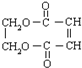
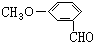 ,有多种同分异构体,其中属于芳香酸的结构简式为:
,有多种同分异构体,其中属于芳香酸的结构简式为: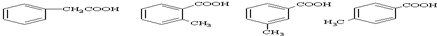 、;
、;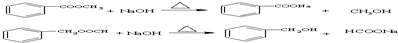 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.1 mol•L-1的醋酸溶液中加水或通入HCl气体都能使$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$值增大 | |
| B. | 0.1 mol•L-1的醋酸钠溶液20 mL与0.1 mol•L-1盐酸10 mL混合后溶液显酸性,则有c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH) | |
| C. | 等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c (Na+)═c (SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | 0.1 mol•L-1某一元酸HA溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×10-8,则该溶液中由水电离出的c(H+)=1×10-11mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝是地壳中含量最多的金属元素,在生活中有广泛的应用,但铝制品不宜长时间盛放腌制食品 | |
| B. | 世博停车场安装催化光解设施,可将汽车尾气中的CO和NOX反应生成无毒物质 | |
| C. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| D. | 高容量的储氢材料研究是推广应用氢氧燃料电池的关键问题之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
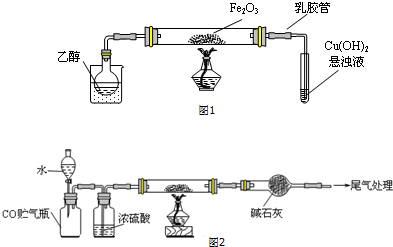
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
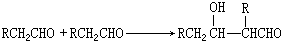
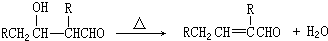

 F:
F: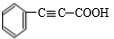

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- | |
| B. | 氯气与水的反应:Cl2+H2O=2H++Cl-+ClO- | |
| C. | 铜片跟稀硝酸反应:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O | |
| D. | 铝片和氢氧化钠溶液反应:Al+OH-+6H2O=[Al(OH)4]-+3H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com