
分析 A、B、C、D均为中学所学的常见物质且均含有同一种元素,
I、若D在火焰上灼烧呈黄色火焰,说明含有钠元素,则A为Na,B为Na2O,C为Na2O2,D为NaOH;
(1)A与水反应是钠和水反应生成氢氧化钠和氢气;
(2)D与铝反应是铝和氢氧化钠溶液反应生成偏铝酸钠和氢气;
Ⅱ、若A气体可使湿润的红色石蕊试纸变蓝,说明为NH3,都含有氮元素,常温下D的浓溶液能使金属Fe、Al钝化则B为NO,C为NO2,D为HNO3,
(1)实验室制备A是利用氢氧化钙固体和氯化铵固体加热反应;
(2)工业上用A制取B是氨气的催化氧化反应生成.
解答 解:A、B、C、D均为中学所学的常见物质且均含有同一种元素,
I、若D在火焰上灼烧呈黄色火焰,说明含有钠元素,则A为Na,B为Na2O,C为Na2O2,D为NaOH;
(1)A与水反应是钠和水反应生成氢氧化钠和氢气,反应的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;
(2)D与铝反应是铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
Ⅱ、若A气体可使湿润的红色石蕊试纸变蓝,说明为NH3,都含有氮元素,常温下D的浓溶液能使金属Fe、Al钝化则B为NO,C为NO2,D为HNO3,
(1)实验室制备A是利用氢氧化钙固体和氯化铵固体加热反应,反应的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(2)工业上用A制取B是氨气的催化氧化反应生成,反应的化学方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
点评 本题考查了无机物推断,根据物质的颜色、物质的性质进行推断,A能连续被氧化,说明A中存在的某种元素有多种化合价,再结合D的性质分析解答,题目难度中等.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:选择题
| A. | 断开1 mol O-O键比断开1 mol N-N键所需能量少448 kJ | |
| B. | 断开1 mol H-O键比断开1 mol H-N键所需能量相差约72.6 kJ | |
| C. | 由以上键能的信息可知H2O的沸点比NH3高 | |
| D. | 由元素非金属性的强弱可知 H-O键比H-N键弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
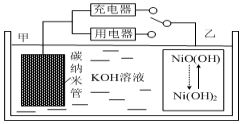 2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )
2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )| A. | 放电时,甲电极为正极,OH-移向乙电极 | |
| B. | 充电时,乙电极反应为:NiO(OH)+H2O+e-═Ni(OH)2+OH- | |
| C. | 充电时,电池的碳电极与直流电源的正极相连 | |
| D. | 电池总反应为H2+2NiOOH$?_{充电}^{放电}$2Ni(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl | B. | NaCl、Na2CO3 | C. | NaCl、I2 | D. | NaCl、NaI、Na2CO3 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省德州市高二上10月月考化学试卷(解析版) 题型:填空题
按要求对下图中两极进行必要的联接并填空:
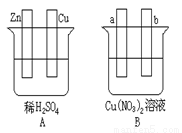
(1)在A图中,使铜片上冒H2气泡。请加以必要联接,电极反应式:锌板: ;铜板: 。
(2)在B图中,a和 b都是石墨电极,使a极析出铜,加以必要的联接后,电极反应式,a极: b极: 。经过一段时间后,停止反应后加入一定量的 ,溶液能恢复至与电解前完全一致。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com