
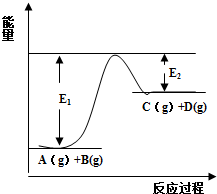
 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.分析 由图象可知,反应物总能量小于生成物总能量,正反应为吸热反应,升高温度,正逆反应速率都增大,加入催化剂,反应热不变,降低反应的活化能,反应速率增大,以此解答.
解答 解:(1)由图象可知,反应物总能量小于生成物总能量,正反应为吸热反应,故答案为:吸热;
(2)升高温度,活化分子百分数增大,正逆反应速率都增大,故答案为:增大;增大;
(3)加入催化剂,反应热不变,故答案为:不影响;
(4)加入催化剂,降低反应的活化能,活化分子百分数增大,反应速率增大,故答案为:减小;减小.
点评 本题考查反应热的判断以及化学反应速率的影响等问题,为高频考点,侧重于学生的分析能力的考查,难度适中,注意催化剂对活化能和反应热的影响.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤可以直接液化,使煤与氢气作用生成液体燃料 | |
| B. | 利用风能、生物能发电,将火力发电用煤进行脱硫处理,有利于环保 | |
| C. | 氮化硅陶瓷、通讯光缆等都是新型无机非金属材料 | |
| D. | 塑料、橡胶、纤维这三大材料都是以石油、煤、天然气为原料生产的 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
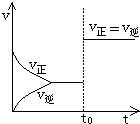 可逆反应aA(g)+bY(g)?cZ(g)在一定温度下的密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(v)-时间(t)的图象图如图所示,下列说法正确的是( )
可逆反应aA(g)+bY(g)?cZ(g)在一定温度下的密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(v)-时间(t)的图象图如图所示,下列说法正确的是( )| A. | 只能通过加入催化剂实现 | B. | 可能通过增大压强来实现 | ||
| C. | 可能通过升高温度实现 | D. | a+b一定不等于c |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
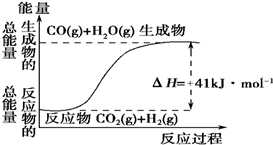
| A. | 其热化学方程式为:CO(g)+H2O(g)═CO2(g)+H2(g)△H=41kJ•mol-1 | |
| B. | 该反应为吸热反应 | |
| C. | 该反应为放热反应 | |
| D. | 若当H2O为液态时反应热为△H2,则△H2>△H |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥⑦ | B. | ④⑥ | C. | ①④⑤⑧ | D. | ④⑥⑦⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com