
| A. | 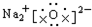 | B. | 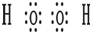 | ||
| C. | 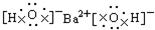 | D. | 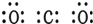 |
分析 A、相同离子不能合并;
B、双氧水为共价化合物;
C、氢氧化钡由2个氢氧根和1个钡离子构成;
D、二氧化碳中碳氧之间为双键.
解答 解:A、氧化钠由2个钠离子和1个氧离子构成,而相同离子不能合并,故氧化钠的电子式为: ,故A错误;
,故A错误;
B、双氧水为共价化合物,H原子和氧原子之间有一对共用电子对,在氧原子和氧原子之间也有一对共用电子对,故电子式为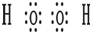 ,故B正确;
,故B正确;
C、氢氧化钡由2个氢氧根和1个钡离子构成,相同离子不能合并,故氢氧化钡的电子式为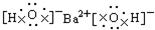 ,故C正确;
,故C正确;
D、二氧化碳中碳氧之间为双键,故电子式为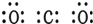 ,故D正确.
,故D正确.
故选A.
点评 本题考查了电子式的书写,在书写电子式之前,先判断化合物为共价化合物还是离子化合物,然后根据不同的方式来书写.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
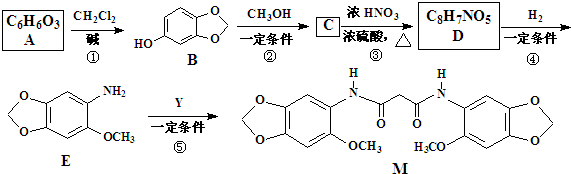

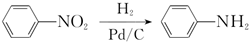
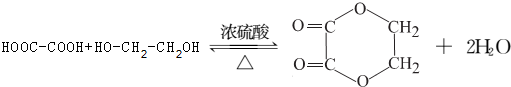 .
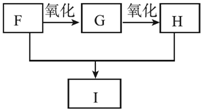
.
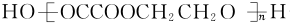 +(2n-1)H2O.
+(2n-1)H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体区别于其它分散系的本质特征是具有丁达尔现象 | |
| B. | 煤的气化、石油分馏、海水制镁、海带提碘等过程中都包含化学变化 | |
| C. | 发酵粉能使焙制出的糕点疏松多孔,是因为发酵粉中含有碳酸氢钠 | |
| D. | 加碘食盐中添加碘酸钾而不用碘化钾,是因为碘酸钾能溶于水而碘化钾不溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸保存在棕色的广口瓶中,并放在阴凉处 | |
| B. | 少量的金属钠应保存在煤油中 | |
| C. | 烧碱溶液放在带玻璃塞的磨口试剂瓶中 | |
| D. | 用做感光材料的溴化银贮存在无色试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫离子的核外电子排布式:1s22s22p63s23p6 | |
| B. | N2的结构式::N≡N: | |
| C. | NaCl的电子式: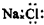 | |
| D. | 原子核内有8个中子的碳原子:${\;}_8^{14}C$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
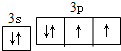 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
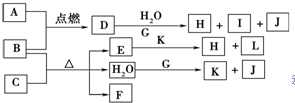 如图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕色烟,B、G为中学化学中常见金属单质,H为红褐色沉淀,I的焰色反应为黄色,组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色.
如图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕色烟,B、G为中学化学中常见金属单质,H为红褐色沉淀,I的焰色反应为黄色,组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com