
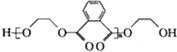
 )的一种工业制法
)的一种工业制法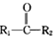 →浓盐酸Zn-HgR1-CH2-R2(其中R1、R2表示烃基或氢原子)
→浓盐酸Zn-HgR1-CH2-R2(其中R1、R2表示烃基或氢原子)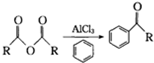 +RCOOH
+RCOOH
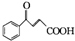 、G
、G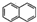 、H
、H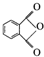 .
.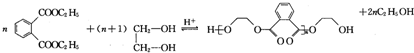 .
.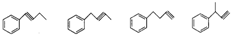 (其中一种).
(其中一种).分析 根据题中各物转化关系,B发生信息Ⅱ的取代反应反应生成C为 ,D发生题中Ⅰ的反应得E为
,D发生题中Ⅰ的反应得E为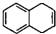 ,根据I的结构和题中信息可知,E与溴发生加成反应得F为
,根据I的结构和题中信息可知,E与溴发生加成反应得F为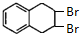 ,F发生消去反应得G为
,F发生消去反应得G为 ,G发生氧化反应得H为
,G发生氧化反应得H为 ,H酸化得I,I发生酯化反应得J,J与乙二醇发生缩聚反应得A,据此答题.
,H酸化得I,I发生酯化反应得J,J与乙二醇发生缩聚反应得A,据此答题.
解答 解:根据题中各物转化关系,B发生信息Ⅱ中的取代反应生成C为 ,D发生题中Ⅰ的反应得E为
,D发生题中Ⅰ的反应得E为 ,根据I的结构和题中信息可知,E与溴发生加成反应得F为
,根据I的结构和题中信息可知,E与溴发生加成反应得F为 ,F发生消去反应得G为
,F发生消去反应得G为 ,G发生氧化反应得H为
,G发生氧化反应得H为 ,H酸化得I,I发生酯化反应得J,J与乙二醇发生缩聚反应得A,
,H酸化得I,I发生酯化反应得J,J与乙二醇发生缩聚反应得A,
(1)E→F的反应为 中的碳碳双键与溴的加成,所用的化学试剂名称为溴水或溴的四氯化碳溶液,
中的碳碳双键与溴的加成,所用的化学试剂名称为溴水或溴的四氯化碳溶液,
故答案为:溴水或溴的四氯化碳溶液;
(2)根据上面的分析可知,反应B→C的反应类型是取代反应,
故答案为:取代反应;
(3)根据上面的分析可知,C为 ,G为
,G为 ,H为
,H为 ,
,
故答案为: 、
、 、
、 ;
;
(4)J→A的化学方程式为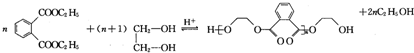 ,
,
故答案为: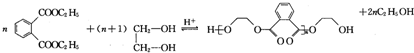 ;
;
(5)E的同分异构体,符合下列条件①除苯环外无其他环状结构 ②苯环上只有一个取代基 ③只有一个官能团 ④能使溴水褪色,则符合条件的同分异构体为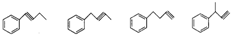 ,有4种,
,有4种,
故答案为:4;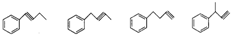 (其中一种).
(其中一种).
点评 本题考查有机合成,题目难度中等,试题涉及有机物的结构、性质、相互转化、方程式和同分异构体的书写等知识,熟练掌握常见有机物结构与性质为解答关键,试题培养了学生的分析、理解能力.


科目:高中化学 来源: 题型:选择题
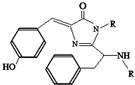 美籍华裔科学家钱永键、日本科学家下修村和美国科学家马丁•沙尔菲因在发现和研究绿色荧光蛋白(GFP)方面做出突出贡献而分享了2008年诺贝尔化学奖.经研究发现GFP中的生色基团结构如图所示,下列有关GFP的说法中正确的( )
美籍华裔科学家钱永键、日本科学家下修村和美国科学家马丁•沙尔菲因在发现和研究绿色荧光蛋白(GFP)方面做出突出贡献而分享了2008年诺贝尔化学奖.经研究发现GFP中的生色基团结构如图所示,下列有关GFP的说法中正确的( )| A. | 该有机物属于芳香烃 | |
| B. | 该有机物能发生水解反应,且1mol该有机物需消耗氢氧化钠2mol | |
| C. | 该有机物能与溴水发生取代反应消耗Br2 3mol | |
| D. | 该有机物既能与盐酸反应,又能与碳酸氢钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在溴乙烷中直接加入AgNO3溶液 | |
| B. | 在溴乙烷中加蒸馏水,然后加入AgNO3溶液 | |
| C. | 在溴乙烷中加入NaOH溶液,加热后酸化,然后加入AgNO3溶液 | |
| D. | 在溴乙烷中加入乙醇加热后,然后加入AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C5H12的同分异构体数目与甲苯(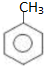 )一氯代物的数目相同 )一氯代物的数目相同 | |
| B. | CH2═CH2+H20$\stackrel{一定条件}{→}$ CH3CH2OH 属于还原反应 | |
| C. | C3H6Cl2有4种同分异构体(不考虑立体异构) | |
| D. | 石油分馏和煤的干馏均属于物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 随着元素原子序数的递增,原子最外层电子总是从1到8重复出现 | |
| B. | 随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现 | |
| C. | 随着元素原子序数的递增,原子半径从小到大(稀有气体除外)发生周期性变化 | |
| D. | 元素原子的核外电子排布、原子半径及元素主要化合价的都发生周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作及现象 | 解释 | |
| A | 鸡蛋白溶液中分别加入NaCl溶液和HgCl2溶液,均有固体析出 | 蛋白质发生了变性 |
| B | 盛放浓NaOH溶液的试剂瓶用玻璃塞久置后,瓶塞很难打开 | NaOH腐蚀玻璃,生成的硅酸钠将瓶口与瓶塞粘在一起 |
| C | 配制FeCl3溶液时加入适量盐酸酸化 | 抑制Fe3+水解,防止所配制溶液变浑浊 |
| D | 二氧化硫通入溴水,溴水褪色 | 说明二氧化硫具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀有气体元素 | |
| B. | 左、下方区域的金属元素 | |
| C. | 右、上方区域的非金属元素 | |
| D. | 金属元素和非金属元素分界线附近的元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com