
【题目】磷是地壳中含量较为丰富的非金属元素,它的单质和化合物在工农业生产中应用广泛。白磷可通过反应 2Ca3(PO4)2+10C→6CaO+P4+10CO 获得。完成下列填空:
(1)磷原子的最外层电子排布式是__________,氧原子核外有______种不同运动状态的电子。C、O两种元素非金属性较强的是_______________。
(2)白磷在空气中露置时间长了会因温度达到____而自燃,使白磷升温的热量主要来自_________。某温度时,在2.0L恒容密闭容器中充入0.5mol PCl5,发生反应PCl5(g)![]() PCl3(g)+Cl2(g)-Q,经过一段时间后达到平衡。
PCl3(g)+Cl2(g)-Q,经过一段时间后达到平衡。
(3)该反应的平衡常数表达式 K=_____________;
(4)其他条件不变,起始时向上述容器中充入1.0 mol PCl5,达到平衡时,PCl5的转化率____(选填“增大”、 “减小”“不变”),平衡常数 K____(选填“增大”、 “减小”“不变”)。
(5)在不同时间(t)测得反应过程中 PCl5 的部分数据如下:
t(s) | 0 | 50 | 100 | 250 | 350 |
n(mol) | 0.5 | 0.42 | 0.41 | 0.40 | 0.40 |
则 100s 时, PCl3的物质的量浓度是__________________。
【答案】 3s23p3 8 O 着火点 白磷氧化 K=[PCl3]·[Cl2]/ [PCl5] 减小 不变 0.045mol/L
【解析】本题主要考查化学平衡。
(1)磷原子的最外层电子排布式是3s23p3,每个电子对应一种运动状态,氧原子核外有8种不同运动状态的电子。同周期元素从左到右非金属性增强,所以C、O两种元素非金属性较强的是O。
(2)白磷在空气中露置时间长了会因温度达到着火点而自燃,使白磷升温的热量主要来自白磷氧化。
(3)该反应的平衡常数表达式K=生成物浓度幂之积与反应物浓度幂之积的比值=[PCl3][Cl2]/[PCl5];
(4)其他条件不变,起始时向上述容器中充入1.0mol PCl5,相当于加压,平衡左移,达到平衡时,PCl5的转化率减小,平衡常数K仅是温度的函数,温度不变,所以K不变。
(5)100s时,n(PCl5)=0.41mol,PCl5减少0.09mol,同时生成PCl30.09mol,所以PCl3的物质的量浓度是0.09mol/2L=0.045mol/L。


科目:高中化学 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义.
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等.已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g)△H1=+489.0kJmol﹣1
C(石墨)+CO2(g)═2CO(g)△H2=+172.5kJmol﹣1
则CO还原Fe2O3的热化学方程式为
(2)某实验将CO2和H2充入一定体积的密闭容器中,在两种不同温度条件下反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=﹣49.0kJmol﹣1
测得CH3OH的物质的量随时间变化如下图所示,回答问题: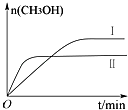
①该反应的平衡常数表达式K=;
②曲线Ⅰ、Ⅱ对应的平衡常数大小关系为:KⅠKⅡ(填“>”、“=”或“<”).
③下列措施中能增大CO2转化率的是 . (填序号)
A.升高温度B.充入He(g)使体系压强增大
C.将H2O(g)从体系中分离 D.再充入一定量CO2
④下列图象正确且能表明在t时刻反应一定处于平衡状态的是 . (填序号)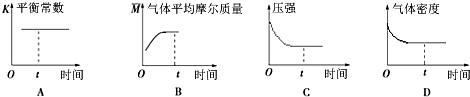
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中,不符合生产实际的是( ) 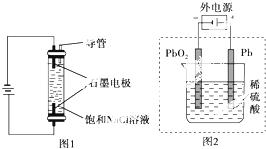
A.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法
B.在镀件上电镀锌,用锌作阳极
C.用如图1装置生产家用消毒液(NaClO)
D.用如图2装置为铅蓄电池充
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对滴有酚酞试液的下列溶液,操作后颜色变深的是( )
A. 明矾溶液加热 B. CH3COONa溶液加热
C. 氨水中加入少量NH4Cl固体 D. 小苏打溶液中加入少量NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.KMnO4 是一种氧化剂,实验室常用 KMnO4和浓盐酸反应制备 Cl2。下图是制备 NaClO溶液的装置图。
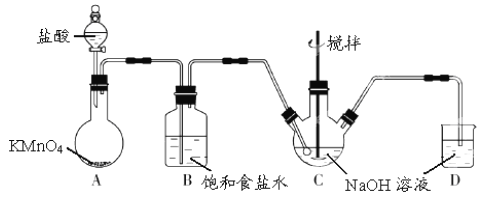
完成下列填空:
(1)KMnO4 稀溶液是一种常见消毒剂,其消毒机理与以下物质相似的是______(选填编号)。
a.75%酒精 b.双氧水 c.NaClO 溶液 d.硫磺皂
(2)B装置中饱和食盐水的作用是___________,D装置中NaOH的作用是______________。
(3)实验操作过程中可调节__________以控制A 装置中产生 Cl2 的气流,C装置需控制反应温度在 0~5℃,实验中可将C 装置放入________________中。
II.测定 KMnO4纯度可用标准 Na2S2O3(式量—158)溶液进行滴定,反应离子方程式为:8MnO4-+5S2O32-+14H+→10SO42-+8Mn2++7H2O。
(4)配制250 mL 0.1000 mol/L标准 Na2S2O3溶液,需准确称取Na2S2O3固体的质量为____g。
(5)取某 KMnO4(式量-158) 产品 0.600g,酸化后用 0.1000 mol/L 标准 Na2S2O3溶液进行滴定,滴定至终点消耗 Na2S2O3溶液 20.00 mL,则该 KMnO4 产品的纯度是_________(保留三位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的说法中,正确的是( )
A.元素周期表有8个主族
B.元素周期表有7个周期
C.IA族的元素全部是金属元素
D.短周期是指第一、二周期
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解.
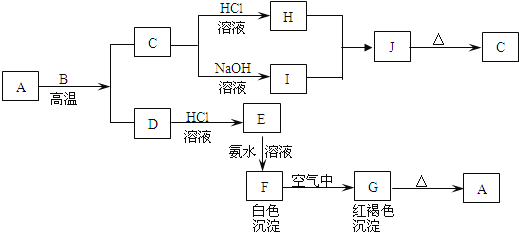
(1)写出下列物质的化学式:A:________,E:________,J:________,G:________.
(2)按要求写方程式:
①A与B在高温条件下生成C和D的化学方程式:________________________________;
②C转化为I的离子方程式:___________________________________________.
③F在空气中转化为G的化学方程式:__________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】减少氮的氧化物和碳的氧化物在大气中的排放是环境保护的重要内容之一。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ/mol
C(s)+O2(g)=CO2(B) △H=-393.5kJ/mol
2C(g)+O2(g)=2CO(g) △H=-221kJ/mol
则:2NO(g)+2CO(g)=N2(g)+2CO2(g) △H=_______。
(2)在密闭容器中充入5molCO和4molNO,发生上述(1)中某反应,如图为平衡时NO的体积分数与温度、压强的关系。回答下列问题:
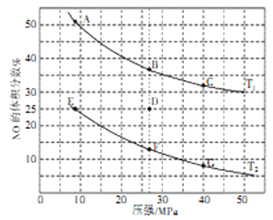
①温度:T1_____T2(填“<”或“>”)。
②某温度下,若反应进行到10分钟达到平衡状态D点时,容器的体积为2L,则此时的平衡常数K=______(保留小数点后两位)。用CO的浓度变化表示起始到平衡的平均反应速率V(CO)=_____。
(3)氮的另一种化合物N2H4(肼)可作制药的原料,也可作火箭的燃料。
①肼的电子式为__________。
②肼能与酸反应。N2H6Cl2溶液呈弱酸性,在水中存在如下反应:
N2H62++H2O=N2H5++H3O+平衡常数K1
N2H5++H2O=N2H4+H3O+平衡常数K2
相同温度下,K1>K2,其主要原因有两个:
a.电荷因素,N2H5+水解程度小于N2H62+;
b.__________________。
(4)肼还可以制备肼一碱性燃料电池,氧化产物为稳定的对环境友好的物质。该电池负极的电极反应式为____________。若以肼一氧气碱性燃料电池为电源,以NiSO4溶液为电镀液,在金属器具上镀镍,开始两极质量相等,当两极质量之差为1.174g时,燃料电池中内电路至少有_______molOH-迁移通过阴离子交换膜。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com