
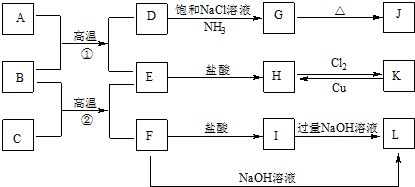
���� BΪ����ɫ��ĩ��ӦΪFe2O3��AΪ��ɫ�ж����壬���ת����ϵ������֪A���л�ԭ�ԣ���AΪCO����DΪCO2��EΪFe��˳�ƿ�֪D���Ȼ�����Һ����ˮ���������Ƽ�еķ�Ӧ����GΪNaHCO3��JΪNa2CO3��H��FeCl2��KΪFeCl3������C����������Ӧ����Fe��F��FΪ����������������ᷴӦ�������������Ʒ�Ӧ��FӦΪAl2O3����C��Al��IΪAlCl3��LΪNaAlO2��������ʵ����ʽ����⣮
��� �⣺BΪ����ɫ��ĩ��ӦΪFe2O3��AΪ��ɫ�ж����壬���ת����ϵ������֪A���л�ԭ�ԣ���AΪCO����DΪCO2��EΪFe��˳�ƿ�֪D���Ȼ�����Һ����ˮ���������Ƽ�еķ�Ӧ����GΪNaHCO3��JΪNa2CO3��H��FeCl2��KΪFeCl3������C����������Ӧ����Fe��F��FΪ����������������ᷴӦ�������������Ʒ�Ӧ��FӦΪAl2O3����C��Al��IΪAlCl3��LΪNaAlO2��
��1����������ķ�����֪��B�Ļ�ѧʽΪ Fe2O3��J�Ļ�ѧʽΪ Na2CO3 ��
�ʴ�Ϊ��Fe2O3�� Na2CO3��
��2����ҵ�Ͻ�����ͨ��ʯ��������ȡƯ�ۣ���Ӧ�Ļ�ѧ��Ӧ����ʽΪ 2Cl2+2Ca��OH��2�TCaCl2+Ca��ClO��2+2H2O��
�ʴ�Ϊ��2Cl2+2Ca��OH��2�TCaCl2+Ca��ClO��2+2H2O��
��3��D��G�Ǻ����Ƽ����Ҫ��Ӧ����Ӧ�Ļ�ѧ����ʽΪNaCl+CO2+NH3+H2O�TNaHCO3+NH4Cl��
�ʴ�Ϊ��NaCl+CO2+NH3+H2O�TNaHCO3+NH4Cl��
��4��K��H������ӡˢ��·�����Ҫ��Ӧ����Ӧ�����ӷ���ʽΪ2Fe3++Cu�T2Fe2++Cu2+��
�ʴ�Ϊ��2Fe3++Cu�T2Fe2++Cu2+��
��5��F��L���������ᴿ�е���Ҫ��Ӧ���÷�Ӧ�����ӷ���ʽΪAl2O3+2 OH-�T2AlO2-+H2O��
�ʴ�Ϊ��Al2O3+2 OH-�T2AlO2-+H2O��
���� ���⿼��������ƶϣ���Ŀ�Ѷ��еȣ�B����ɫ���ƶ�ͻ�ƿڣ��ٽ��ת����ϵ��A�����ʽ����ƶϣ����ؿ���Ԫ�ػ��������ʣ�ѧϰ��ע����գ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2+2Fe3++2H2O�TSO42-+2Fe2++4H+ | |
| B�� | I2+2Fe2+�T2I-+2Fe3+ | |
| C�� | SO2+I2+2H2O�T2I-+4H++SO42- | |
| D�� | ����Cl2ͨ��FeI2��Һ�У�Cl2+2I-�T2Cl-+I2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 2015��8��12�������ش�ը�¹ʣ���һ�����������ǶԻ�������Ĺ�ע���ݲ�Σ���ֿ��д��д������ơ��ء����ף�P4��������狀��軯�ƣ�NaCN����
2015��8��12�������ش�ը�¹ʣ���һ�����������ǶԻ�������Ĺ�ע���ݲ�Σ���ֿ��д��д������ơ��ء����ף�P4��������狀��軯�ƣ�NaCN�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeCl3��Һ�У�K+��Na+��SO42-��SCN- | |
| B�� | ʹ��̪��Һ������Һ�У�NH4+��Na+��HCO3-��NO3- | |
| C�� | Ư����Һ�У�K+��Na+��I-��CO32- | |
| D�� | ������Ӧ������������Һ�У�Na+��K+��CO32-��OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1-��������������ص��Ҵ���Һ���ȣ�CH3CH2CH2Br+KOH$��_{��}^{�Ҵ�}$CH3CH2CH2OH+KBr | |
| B�� | ������������H218O��ϡ�����ֻ�ϲ����ȣ�CH3COOCH2CH3+H218O$��_{��}^{ϡ����}$CH3COOH+CH3CH218OH | |
| C�� | ��ʳ�׳�ȥˮƿ���ˮ����CaCO3+2H+=Ca2++H2O+CO2�� | |
| D�� | ��������Һ������ȩ�е�ȩ����CH3CHO+2Ag��NH3��2++2OH$��_{��}^{ˮԡ}$CH3COO-+NH4++3NH3+2Ag��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 1��2-��������������Ϳ����������Ӽ���������������ɫҺ�壬�е�131.4�棬�۵�9.79�棬������ˮ�������ڴ����ѡ���ͪ���л��ܼ�����ʵ���п�����ͼ9��ʾװ���Ʊ�1��2-�������飮���з�Һ©������ƿa��װ���Ҵ���Ũ����Ļ��Һ���Թ�d��װ��Ũ�壨���渲������ˮ��������д���пհף�
1��2-��������������Ϳ����������Ӽ���������������ɫҺ�壬�е�131.4�棬�۵�9.79�棬������ˮ�������ڴ����ѡ���ͪ���л��ܼ�����ʵ���п�����ͼ9��ʾװ���Ʊ�1��2-�������飮���з�Һ©������ƿa��װ���Ҵ���Ũ����Ļ��Һ���Թ�d��װ��Ũ�壨���渲������ˮ��������д���пհף��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com