
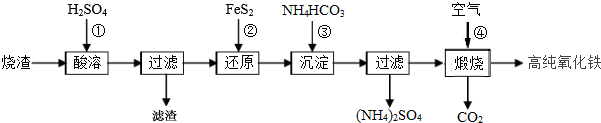
���� ����������Ҫ�ɷ�ΪFe2O3��Fe3O4��FeO��SiO2���м������ᣬ����������ת��Ϊ�����ӡ��������ӣ�SiO2�����ᷴӦ�����˺���������ΪSiO2����Һ�м���FeS2��Fe3+��ԭΪFe2+�����˺�����Һ�м���̼����刺�����FeCO3���������տɵ�Fe2O3����Һ�����Ϊ��Σ�����Ϊ����ʩ�ã�
��1�����������顢���������H2SO4��Ŀ���������Ԫ�صĽ����ʣ�ͬʱ���������ӵ�ˮ�⣬���ʱFe2O3��Fe3O4��FeO����ϡ���ᷴӦ�õ�Fe2+��Fe3+��SiO2������ϡ���ᷴӦ��
��2����Һ�м���FeS2��Fe3+��ԭΪFe2+��-1�۵���������+6�۵����ݵ�ʧ�����غ㡢ԭ���غ�͵���غ���д���ӷ�Ӧ����ʽ��
��3������NH4HCO3Ŀ�����к���Һ�е��ᣬ������Һ��pH��ʹFe2+ȫ��ת��ΪFeCO3��������������pHֵΪ7.6����ת��Ϊ�������������������˵�̼����������Һ��������泥����Լ���FeCO3�Ƿ�ϴ�������Ǽ���ϴ����Һ���Ƿ�����������ӣ�����������������ų�̼������ӵĸ��ţ�
��4���������̿�֪���պ�IJ���Ϊ������̼��ͬʱ�õ�������������ԭ���غ���д��ѧ��Ӧ����ʽ��
��� �⣺��1����������Ҫ�ɷ�ΪFe2O3��Fe3O4��FeO��SiO2�������ʱFe2O3��Fe3O4��FeO����ϡ���ᷴӦ�õ�Fe2+��Fe3+�����ʱ�����轫�������飬ͨ������Ӵ������
�����Ԫ�صĽ����ʣ����������ӡ������Ӷ���ˮ������ԣ�ͨ���������H2SO4�����������ӵ�ˮ�⣬SiO2������ϡ���ᷴӦ�������������˺�������Ҫ�ɷ�ΪSiO2��
�ʴ�Ϊ�������Ԫ�صĽ����ʣ�ͬʱ���������ӵ�ˮ�⣻SiO2��
��2����Һ�м���FeS2��Fe3+��ԭΪFe2+��-1�۵���������+6�۵���FeS2��SO42-��ʧȥ14e-��Fe3+��Fe2+���õ�e-����С������Ϊ14�����ݵ�ʧ�����غ㡢ԭ���غ�͵���غ㣬���ӷ�Ӧ����ʽΪ��FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+��
�ʴ�Ϊ��FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+��
��3��NH4HCO3�ܺ��ᷴӦ����狀Ͷ�����̼��ͬʱ�ܵ�����Һ��PH��ʹFe2+ȫ��ת��ΪFeCO3��������������pHֵΪ7.6����ת��Ϊ���������������������Ʊ�FeCO3Ӧ������ҺpH���˹��ߣ��������������������������˵�̼����������Һ��������泥����Լ���FeCO3�Ƿ�ϴ�������Ǽ���ϴ����Һ���Ƿ�����������ӣ����Բ���Ϊȡ���һ��ϴ����Һ���μ������ữ�ų�̼������ӵĸ��ţ��μ������ữ���Ȼ�����Һ�����������ɣ�˵��ϴ�Ӹɾ���
�ʴ�Ϊ���к���Һ�е��ᣬ������Һ��pH��ʹFe2+ȫ��ת��ΪFeCO3��Fe��OH��2��ȡ���һ��ϴ��Һ���������Թܣ��μ������ữ���Ȼ�����Һ�����������ɣ�˵��ϴ�Ӹɾ���
��4���������̿�֪���պ�IJ���Ϊ������̼��ͬʱ�õ�����������������ΪFe2O3��CO2����Ӧ��Ϊ̼���κ����������Ի�ѧ��Ӧ����ʽΪ��4FeCO3+O2$\frac{\underline{\;����\;}}{\;}$2Fe2O3+4CO2��
�ʴ�Ϊ��4FeCO3+O2$\frac{\underline{\;����\;}}{\;}$2Fe2O3+4CO2��
���� ���⿼�����ʵ��Ʊ��ͷ��������������ѧ������������ʵ���������ۺ����û�ѧ֪ʶ�����Ŀ��飬Ϊ�߿��������ͣ���Ŀ�Ѷ��еȣ�ע�����ʵ�������Լ�������ʵ����ʽ����⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ı�ȼ����Ϊ-890.3 kJ•mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2O2��g���TCO2��g��+2H2O ��g����H=-890.3 kJ•mol-1 | |
| B�� | ��ͬ�����£�2mol��ԭ�������е�����С��1mol����������е����� | |
| C�� | �����£���ӦC��s��+CO2��g���T2CO��g�� �����Է����У���÷�Ӧ�ġ�H��0 | |
| D�� | ��֪��2H2��g��+O2��g���T2H2O ��g����H1=a kJ•mol-1��2H2��g��+O2��g���T2H2O ��l����H2=b kJ•mol-1����a��b |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 | Mn��OH��2 |
| ��ʼ���� | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| ��ȫ���� | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
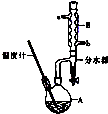 B�����ѳ������л���Ӧ���ܼ���ʵ�����Ʊ������ѵķ�Ӧ����Ҫʵ��װ�����£�
B�����ѳ������л���Ӧ���ܼ���ʵ�����Ʊ������ѵķ�Ӧ����Ҫʵ��װ�����£�| ��Է������� | �е�/�� | �ܶȣ�g/cm3�� | ˮ���ܽ��� | |
| ������ | 74 | 117.2 | 0.819 | �� |
| ������ | 130 | 142.0 | 0.7704 | �������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���롢�ᴿ��ȷ����ѧʽ��ȷ��ʵ��ʽ��ȷ���ṹʽ | |
| B�� | ���롢�ᴿ��ȷ���ṹʽ��ȷ��ʵ��ʽ��ȷ����ѧʽ | |
| C�� | ���롢�ᴿ��ȷ��ʵ��ʽ��ȷ����ѧʽ��ȷ���ṹʽ | |
| D�� | ȷ����ѧʽ��ȷ��ʵ��ʽ��ȷ���ṹʽ�����롢�ᴿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
| �� ���� | �� | �� | �� | �� | �� | �� | �� | 0 |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | �� | �� | |
| 4 | �� | ⑪ | ⑫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

| ѹǿ/Mpa C% �¶�/�� | 0.1 | 10 | 20 |
| 200 | 15.3 | 81.5 | 86.4 |
| 300 | 2.2 | a | 64.2 |
| 400 | 0.4 | 25.1 | 38.2 |
| 500 | 0.1 | 10.6 | 19.1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com