
| A����ͭƬ���뵽FeCl3��Һ�У��۲���Һ��ɫ�ı仯��֤������������Fe3+��Cu2+��Cu+2Fe3+=Cu2++2Fe2+ |
| B���ⶨ0.1mol/LH3PO4��Һ��pH��1֤��H3PO4Ϊ���H3PO4?3H++PO43�� |
| C��ʵ������Na2O2��H2O��Ӧ�������Ʊ�O2��Na2O2+H2O=2Na++2OH-+O2�� |
| D����Na2CO3��Һ�е��������Һ����Һ��ƣ�֤��Na2CO3��Һ�Լ��ԣ�CO32��+H2O?HCO3��+OH�� |


 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
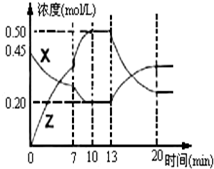 I����1L������ͨ��CO2��H2��2mol����һ�������·�����Ӧ��CO2+H2?CO+H2O���ش��������⣺
I����1L������ͨ��CO2��H2��2mol����һ�������·�����Ӧ��CO2+H2?CO+H2O���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ӳ֬�������������������� |
| B����������֬�� |
| C���������Ҷ��� |
| D����ϩ����Ӳ֬�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��HCl |
| B��H2SO4 |
| C��CH3COOH |
| D��H3PO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��H+��S��K+��Cl2 |
| B��Fe2+��Zn��S2-��C |
| C��Fe3+��I-��H2��CO |
| D��Al��Zn2+��Na��I- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
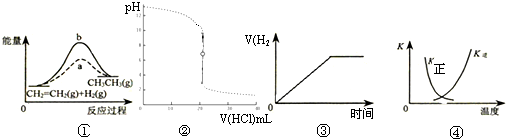
| A��ͼ����a��b���߷ֱ��ʾ��ӦCH2=CH2��g��+H2��g����CH3CH3��g��+Qʹ�ú�δʹ�ô���ʱ����Ӧ�����е������仯 |
| B��ͼ�ڱ�ʾ25��ʱ����0.1mol?L-1����ζ�20mL 0.1mol?L-1 NaOH��Һ����Һ��pH�����������ı仯 |
| C��ͼ�۱�ʾп�������ϡ���ᷴӦʱ��V��H2�� ��ʱ��ı仯ͼ |
| D��ͼ�������߱�ʾ��Ӧ2SO2��g��+O2��g��=2SO3��g��+Q �����淴Ӧ��ƽ�ⳣ��K���¶ȵı仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��SO2��g��+
| ||||
| B��2SO2��g��+O2��g���T2SO3��g����H1�����H1����H����H��ֵ��A������� | ||||
| C��X��g��+Y��g���TZ��g��+W��s����H��0��ƽ������X����H���� | ||||
| D��X��g��+Y��g���TZ��g��+W��s����H��0��ƽ����������Z���ų����������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com