
【题目】(1)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是______mol。
(2)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是________,又变为棕黄色的原因是用离子方程式解释___________________________.
(3)在100mLFeBr2溶液中通入标况下2.24LCl2,溶液溶液中有1/4的Br- 被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为_________________。
(4)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式_________。向反应后的溶液中通入过量CO2,反应的离子方程式为______。
(5)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式___________,反应中生成0.2mol HNO3,转移的电子数目为_______。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是________
【答案】0.032 2Fe3++SO32-+H2O=2Fe2++SO42-+2H+ 3Fe2++4H++NO3-=3Fe3++NO↑+2H2O ![]() mol/L或1.33mol/L NaAlO2 AlO2-+ CO2+ 2H2O= Al(OH)3↓+HCO3- 3NF3+5H2O=2NO+HNO3+9HF 0.4NA 出现红棕色气体
mol/L或1.33mol/L NaAlO2 AlO2-+ CO2+ 2H2O= Al(OH)3↓+HCO3- 3NF3+5H2O=2NO+HNO3+9HF 0.4NA 出现红棕色气体
【解析】
(1)n(KI)=0.06mol,与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则n(I2)=n(KIO3)=0.02mol,共失去电子的物质的量为2×0.02mol+0.02mol×[5-(-1)]=0.16mol,则消耗KMnO4的物质的量的是![]() =0.032mol,
=0.032mol,
故答案为:0.032;
(2)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,原因是Fe3+与SO32-发生氧化还原反应生成Fe2+和SO42-,反应的离子方程式为2Fe3++SO32-+H2O=2Fe2++SO42-+2H+,反应后溶液呈酸性,则在酸性条件下NO3-与Fe2+反应生成Fe3+,过一会又变为棕黄色,反应的离子方程式为:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O,
故答案为:2Fe3++SO32-+H2O=2Fe2++SO42-+2H+;3Fe2++4H++NO3-=3Fe3++NO↑+2H2O;
(3)n(Cl2)=![]() =0.1mol,设原FeBr2溶液中FeBr2的物质的量浓度为x,由还原性Br-<Fe2+,液溶液中有
=0.1mol,设原FeBr2溶液中FeBr2的物质的量浓度为x,由还原性Br-<Fe2+,液溶液中有![]() 的Br-被氧化成单质Br2,则亚铁离子全部被氧化,由电子守恒可知,0.1L×x×(3-2)+0.1L×x×2×
的Br-被氧化成单质Br2,则亚铁离子全部被氧化,由电子守恒可知,0.1L×x×(3-2)+0.1L×x×2×![]() ×(1-0)=0.1mol×2×(1-0),解得x=
×(1-0)=0.1mol×2×(1-0),解得x=![]() mol/L,
mol/L,
故答案为:![]() mol/L或1.33mol/L;
mol/L或1.33mol/L;
(4)Al、Al2O3和Al(OH)3都可与NaOH溶液反应,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,氢氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,反应后溶液中溶质的化学式NaAlO2。向反应后的溶液中通入过量CO2,反应的离子方程式为AlO2-+ CO2+ 2H2O= Al(OH)3↓+HCO3-。
答案为:NaAlO2;AlO2-+ CO2+ 2H2O= Al(OH)3↓+HCO3-;
(5)①NF3→NO,化合价降低1价,被还原,NF3→HNO3,化合价升高2价,被氧化,由反应物和生成物可写出反应的化学方程式为3NF3+5H2O=2NO+HNO3+9HF;反应中生成0.2molHNO3,转移的电子数目为0.2mol×2=0.4mol=0.4NA;
故答案为:3NF3+5H2O=2NO+HNO3+9HF;0.4NA;
②NF3无色、无臭,但一旦在空气中泄漏,会与空气中的水蒸气反应生成NO,NO易与空气中氧气反应生成红棕色的NO2气体,判断该气体泄漏时的现象是出现红棕色气体;
故答案为:出现红棕色气体;


科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有Na+、K+、NH4+、Mg2+、Cu2+、SO42-、SO32-、Cl-、Br-、CO32-中的若干种,离子浓度都为0.1mol·L-1。往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如下实验:

则关于原溶液的判断不正确的是
A.若步骤中Ba(NO3)2和HNO3溶液改用BaCl2和盐酸的混合溶液,则对溶液中离子的判断无影响
B.无法确定原溶液中是否存在Cl-
C.肯定存在的离子是SO32-、Br-,是否存在Na+、K+需要通过焰色反应来确定
D.肯定不存在的离子是Mg2+、Cu2+、SO42-、CO32-,是否含NH4+另需实验验证
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取10g粗铁加入足量稀硫酸中,共收集到5.6L氢气(标准状况),则粗铁中混有的杂质不可能是( )
A. Cu和Mg B. Mg和Al C. Al 和 Si D. SiO2和Zn
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备下列物质的生产流程合理的是( )
A. 由铝土矿冶炼铝:铝土矿![]() Al2O3
Al2O3![]() AlCl3
AlCl3![]() Al
Al
B. 从海水中提取镁:海水![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
C. 由NaCl制漂白粉:饱和食盐水![]() Cl2
Cl2![]() 漂白粉
漂白粉
D. 由黄铁矿制硫酸:黄铁矿![]() SO2
SO2![]() SO3
SO3![]() H2SO4
H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如图,下列叙述错误的是( )
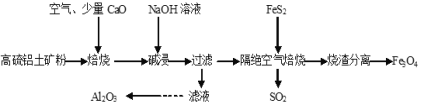
A.烧渣分离可以选择用磁铁将烧渣中的Fe3O4分离出来
B.隔绝空气焙烧时理论上反应消耗的n(FeS2)∶n(Fe2O3)=1∶5
C.向滤液中通入过量CO2、过滤、洗涤、灼烧沉淀可制得Al2O3
D.加入CaO可以减少SO2的排放同时生成建筑材料CaSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液Y的可能含有Na+、Fe3+、Ba2+、NH4+、Cl-、SO42-、HCO3-、HSO3-中的几种离子,溶液中阳离子浓度相同。为了确定其组成,某同学进行了如下实验(假设气体均全部逸出,忽略H2O2的分解)下列说法不正确的是
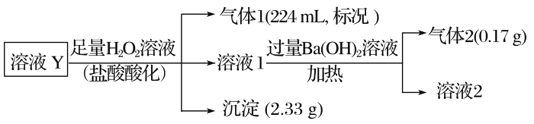
A.溶液Y中一定不存在Fe3+、SO42-
B.溶液Y中一定含有Cl-,且n(Cl-)=001mol
C.沉淀中肯定只含有BaSO4
D.溶液Y中可能存在Na+,为确定是否存在,可取溶液1通过焰色反应实验验证
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,KHS溶液里存在下列平衡:a.HS-+H2O ![]() H3O++S2- b.HS-+H2O
H3O++S2- b.HS-+H2O![]() OH-+H2S。
OH-+H2S。
(1)平衡a是_______平衡(填“电离”或“水解”,下同),平衡b是_______平衡。
(2)向KHS溶液中加入少量NaOH固体,c(S2-)将__________(填“增大”、“减小”或“不变”,下同),向KHS溶被中通入HCl时,c(HS-)将__________。
(3)向KHS溶液中加入CuSO4溶液,有黑色沉淀(CuS)产生,则平衡a__________移动(填“正向”、“逆向”或“不”,下同),平衡b__________移动。
(4)在KHS溶液中,c(OH-)-c(H+)=____________________。
(5)向KHS溶液中加入AlCl3溶液,产生的现象为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C均为中学化学常见的纯净物,它们之间存在如下转化关系,其中①②③均为有单质参与的反应。
![]()
(1)若A是常见的金属,①③中均有同一种气态非金属单质参与反应,B溶液遇KSCN显血红色,且②为化合反应,写出反应②的离子方程式________。
(2)若B是太阳能电池用的光伏材料,①②③为工业制备B的反应。C的化学式是______,写出反应①的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奶油中有一种只含C、H、O的化合物A。A相对分子质量为88,分子中C、H、O原子个数比为2:4:1。
(1)A的分子式为______________。
已知:①ROH+HBr(氢溴酸)![]() RBr+H2O
RBr+H2O
②

A中含有碳氧双键,与A相关的反应如下:已知一分子B可以转化为两分子C。

(2)写出A→E、E→F的反应类型:A→E_____________、E→F______________。
(3)写出C、F的结构简式:C__________________、F_______________。
(4)写出B→D反应的化学方程式____________________________。
(5)A的同分异构体中含有 结构的共有___________种,写出其中一种能够发生银镜反应的物质的结构简式:____________________。(不考虑立体异构)
结构的共有___________种,写出其中一种能够发生银镜反应的物质的结构简式:____________________。(不考虑立体异构)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com