
| A. | I2仅是还原产物 | |
| B. | Cu(IO3)2既是氧化剂又是还原剂 | |
| C. | 氧化产物与还原产物物质的量比为13:2 | |
| D. | 当1 mol氧化剂参加反应时,被氧化的物质的物质的量为11mol |
分析 该反应中Cu元素化合价由+2价变为+1价、Cu(IO3)2中碘元素化合价由+5价变为0价、KI中有$\frac{11}{12}$的I元素化合价由-1价变为0价,转移电子数为22,
A.氧化剂对应的产物是还原产物,还原剂对应的产物是氧化产物;
B.失电子的反应物是还原剂、得电子的反应物是氧化剂;
C.CuI是还原产物,有$\frac{11}{13}$的碘是氧化产物,有$\frac{2}{13}$的碘是还原产物;
D.1mol氧化剂在反应中得到的电子为1mol×(2-1)+2mol×(5-0)=11mol,根据转移电子相等计算.
解答 解:该反应中Cu元素化合价由+2价变为+1价、Cu(IO3)2中碘元素化合价由+5价变为0价、KI中有$\frac{11}{12}$的I元素化合价由-1价变为0价,转移电子数为22,
A.氧化剂对应的产物是还原产物,还原剂对应的产物是氧化产物,所以碘是氧化产物和还原产物,故A错误;
B.失电子的反应物是还原剂、得电子的反应物是氧化剂,因为Cu(IO3)2中Cu、I元素都得电子,所以只是氧化剂,故B错误;
C.CuI是还原产物,有$\frac{11}{13}$的碘是氧化产物,有$\frac{2}{13}$的碘是还原产物,所以氧化产物与还原产物物质的量比为11:4,故C错误;
D.1mol氧化剂在反应中得到的电子为1mol×(2-1)+2mol×(5-0)=11mol,KI中I元素的化合价由-1价升高为0,则KI为还原剂被氧化,所以当1mol氧化剂参加反应时,被氧化的物质的物质的量为11mol,故D正确;
故选D.
点评 本题考查氧化还原反应,为高频考点,侧重考查学生分析判断及计算能力,明确氧化产物和还原产物成分及KI作氧化剂和还原剂的物质的量之比是解本题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 工业上用电解MgCl2溶液的方法冶炼Mg | |
| B. | 钢铁发生吸氧腐蚀的正极反应式为4OH--4e-═O2↑+2H2O | |
| C. | 如图中发生反应的方程式为:Fe+2H+=Fe2++H2↑ | |
| D. | 碱性锌锰干电池放电时的正极反应为:MnO2+H2O+e-=MnOOH+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石和晶体硅 | B. | CO2和SiO2 | C. | KCl和HBr | D. | NaOH和NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
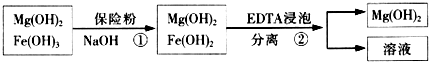
| 精制阻燃剂的条件 | 阻燃剂铁含量 | |||
| 序号 | 提纯体系温度/℃ | 加入EDTA质量/g | 加入保险粉质量/g | W(Fe)/(10-4g) |
| 1 | 40 | 0.05 | 0.05 | 7.63 |
| 2 | 40 | 0.05 | 0.10 | 6.83 |
| 3 | 60 | 0.05 | 0.10 | 6.83 |
| 4 | 60 | 0.10 | 0.10 | 6.51 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
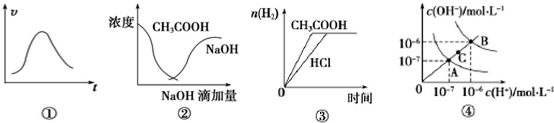
| A. | 图①可表示一定条件下,锌和稀硫酸反应的速率随时间变化的趋势图 | |
| B. | 图②中曲线表示将氢氧化钠溶液滴加到醋酸溶液中浓度的变化趋势图 | |
| C. | 图③表示等体积、等物质的量浓度的盐酸和醋酸,分别加足量镁粉,产生H2的物质的量变化 | |
| D. | 图④为水的电离平衡曲线图,若从A点到C点,可采用升高温度的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
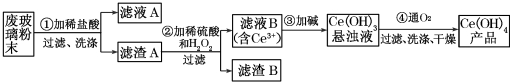
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com