
| A. | 明矾和氢氧化钡溶液 | B. | 钠和MgC12溶液 | ||
| C. | 铜粉和FeC13溶液 | D. | Na2O2和少量FeCl2溶液 |
分析 A.发生复分解反应生成硫酸钡沉淀;
B.钠与水反应生成氢气和NaOH,NaOH与氯化镁生成氢氧化镁沉淀;
C.铜粉和FeC13溶液生成氯化铜和氯化亚铁;
D.过氧化钠与水反应生成氧气和NaOH,FeCl2被氧化,与NaOH反应生成氢氧化铁沉淀.
解答 解:A.明矾和氢氧化钡溶液,当氢氧化钡过量反应只生成硫酸钡沉淀,只观察到白色沉淀,故A不选;
B.钠与水反应生成氢气和NaOH,NaOH与氯化镁生成氢氧化镁白色沉淀,则既产生无色气体,又生成白色沉淀,故B选;
C.铜粉和FeC13溶液生成氯化铜和氯化亚铁,没有气体生成,也无沉淀生成,故C不选;
D.过氧化钠与水反应生成氧气和NaOH,FeCl2被氧化,与NaOH反应生成氢氧化铁红褐色沉淀,既产生无色气体,又生成红褐色沉淀,故D不选;
故选B.
点评 本题考查物质的性质及相互转化,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的综合应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | 电解熔融氧化铝:2Al2O3(熔融)$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑ | |
| C. | NaHCO3溶液与稀H2SO4反应:HCO3-+H+═H2O+CO2↑ | |
| D. | 向Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2AlCl3(熔融) $\frac{\underline{\;电解\;}}{冰晶}$ 4Al+3Cl2↑ | |
| B. | Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2 | |
| C. | Fe+CuSO4═FeSO4+Cu | |
| D. | 2KCl(熔融)$\frac{\underline{\;电解\;}}{\;}$2K+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 消除制硝酸工业尾气中的氮氧化物的污染:NO+NO2+2NaOH═2NaNO2+H2O | |
| B. | 消除硫酸厂尾气中的SO2:SO2+2NH3•H2O═(NH4)2SO3+H2O | |
| C. | 用反应: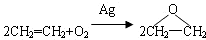 制备环氧乙烷 制备环氧乙烷 | |
| D. | 制CuSO4:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
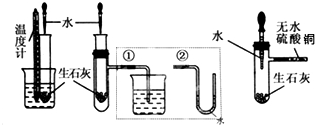
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 解释或结论 |
| A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,溶液褪色 | SO2具有漂白性 |
| B | 将NaHCO3和NaAlO2溶液混合产生白色沉淀 | 酸性:HCO3->Al(OH)3 |
| C | 某钾盐溶于盐酸,产生无色无味气体,该气体通入 澄清石灰水,有白色沉淀出现 | 该钾盐是K2CO3 |
| D | NaI溶液$\stackrel{30%H_{2}O_{2}溶液}{→}$$\stackrel{稀硝酸及淀粉}{→}$溶液变蓝色 | 酸性条件下H2O2的氧化性比I2强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
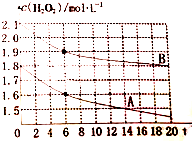 现有如下溶液:①1.0mL0.10mol•L-1双氧水 ②1.0mL0.20mol•L-1双氧水 ③3.0mL0.10mol•L-1KMnO4溶液 ④3.0mL0.010mol•L-1KMnO4溶液.所有实验均需加入1.0mL稀硫酸(足量),依据褪色时间长短判定反应速率快慢:
现有如下溶液:①1.0mL0.10mol•L-1双氧水 ②1.0mL0.20mol•L-1双氧水 ③3.0mL0.10mol•L-1KMnO4溶液 ④3.0mL0.010mol•L-1KMnO4溶液.所有实验均需加入1.0mL稀硫酸(足量),依据褪色时间长短判定反应速率快慢:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 降低温度可以缩短反应达到平衡的时间 | |
| B. | 恒容时通入氩气,压强增大,平衡向右移动 | |
| C. | 恒容时通入X2,平衡向正反应方向移动,平衡常数不变 | |
| D. | 恒温恒压下,若混合气体密度不变,说明反应已达平衡 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com