
科目:高中化学 来源:2016-2017学年海南省琼海市高一上学期第一次月考化学试卷 题型:选择题
设NA为阿伏伽德罗常数的值,下列有关说法不正确的是
A.常温下,48gO3含有的氧原子数3NA
B.标准状况下,33.6LCO中含有的原子数是3NA
C.0.5mol·L-1CaCl3溶液中含Cl-数目为NA
D.17gNH3所含的电子数为10NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年遵义市高二上学期期中考试化学(文)试卷 题型:选择题
人体内所必需的下列元素中,因摄 入量不足而导致骨质疏松的是
入量不足而导致骨质疏松的是
A.K
B.Ca
C.Na
D.Fe
查看答案和解析>>
科目:高中化学 来源:2016-2017学年遵义市高二上学期期中考试化学(文)试卷 题型:选择题
下列关于油脂的叙述中,不正确的是
A.油脂属于酯类
B.油脂没有固定的熔沸点
C.油脂是高级脂肪酸的甘油酯
D.油 脂都不能使溴水褪色
脂都不能使溴水褪色
查看答案和解析>>
科目:高中化学 来源:2016-2017学年遵义市高二上学期期中考试化学(文)试卷 题型:选择题
过量的锌粉与一定量的稀盐酸反应,为了减慢反应速率,但是又不影响生成的氢气总量,可以采取的措施是
A.升高温度
B.加入适量的水
C.加入少量CuSO4溶液
D.加入浓度较大的盐酸
查看答案和解析>>
科目:高中化学 来源:2016-2017学年遵义市高二上学期期中考试化学(文)试卷 题型:选择题
根据元素在周期表中的位置判断,下列元素中原子半径最小的是
A. 氧
B. 氟
C. 碳
D. 氮
查看答案和解析>>
科目:高中化学 来源:2016-2017学年遵义市高二上学期期中考试化学(文)试卷 题型:选择题
下列物质中常温下既能与NaOH溶液反应,又能与盐酸反应产生氢气的是
A.Mg
B.Cl2
C.Si
D.Al
查看答案和解析>>
科目:高中化学 来源:2016-2017学年遵义市高二上学期期中考试(理科)化学试卷 题型:选择题
已知:C(s)+CO2(g) 2CO(g)△H>0。该反应的达到平衡后,下列条件
2CO(g)△H>0。该反应的达到平衡后,下列条件
有利于反应向正方向进行的是
A.升高温度和 减小压强
减小压强
B.降低温度和减小压强
C.降低温度和增大压强
D.升高温度和增大压强
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上第二次月考化学试卷(解析版) 题型:实验题
某化学小组探究酸性条件下NO3-、SO42-、Fe3+三种微粒的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
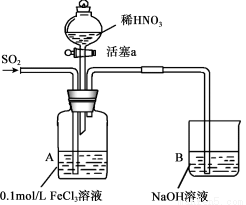
实验记录如下:
实验序号 | 实验操作 | 实验现象 |
I | 向A装置中通入一段时间的SO2气体。 | A中黄色溶液迅速变成深红棕色,最终变为浅绿色。 |
II | 取出少量A装置中的溶液,先加入KSCN溶液,再加入BaCl2溶液。 | 加入KSCN溶液后溶液不变色,再加入BaCl2溶液产生白色沉淀。 |
III | 打开活塞a,将过量稀HNO3加入装置A中,关闭活塞a | A中浅绿色溶液最终变为黄色。 |
IV | 取出少量A装置中的溶液,加入KSCN溶液;向A装置中通入空气。 | 溶液变为红色;液面上方有少量红棕色气体生成。 |
请回答下列问题:
(1)配制FeCl3溶液时,常常加入盐酸,目的是(用化学方程式和简单文字叙述): 。
(2)资料表明,Fe3+能与SO2结合形成深红棕色物质Fe(SO2)63+,反应方程式为: Fe3+ + 6SO2  Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因 。
Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因 。
(3)实验II中发生反应的离子方程式是 。
(4)实验III中,浅绿色溶液变为黄色的原因是(用离子方程式表示) 。
(5)实验IV中液面上方有少量红棕色气体生成,发生反应的方程式是 。
(6)综合上述实验得出的结论是:在酸性条件下,NO3-、SO42-、Fe3+三种微粒的氧化性由强到弱的顺序是: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com