



| 6×2+2-6 |
| 2 |
| 10×2+2-8 |
| 2 |
| 6×2+2-6 |
| 2 |
| 10×2+2-8 |
| 2 |
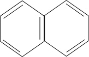 ,故答案为:c;
,故答案为:c;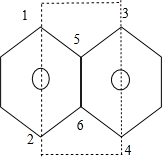 ,1、2碳原子处于右边苯环氢原子位置,3、4碳原子处于左边苯环氢原子位置,5、6碳原子共用,苯为平面结构,所以萘是平面结构,所有原子处于同一平面,故c正确;
,1、2碳原子处于右边苯环氢原子位置,3、4碳原子处于左边苯环氢原子位置,5、6碳原子共用,苯为平面结构,所以萘是平面结构,所有原子处于同一平面,故c正确;

科目:高中化学 来源: 题型:

| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 | |
| 第一次称量 | 第二次称量 | ||
| 11.710g | 22.700g | 18.621g | a |
查看答案和解析>>
科目:高中化学 来源: 题型:
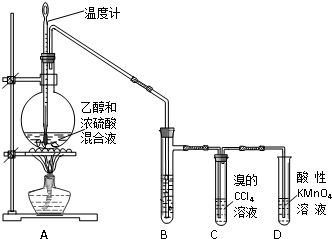
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移电子总数为0.1mol |
| B、明矾溶于水形成的Al(OH)3胶体能吸附水中悬浮物,所以明矾可用于水的净化 |
| C、向Na2CO3溶液中滴加盐酸溶液,一定有CO2气体生成 |
| D、Na2O2常用于潜水艇或呼吸面具的供氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、20% | B、25% |
| C、75% | D、80% |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com