
下列说法中错误的是( )
|
| A. | 从1L 1mol•L﹣1的NaCl溶液中取出10mL,其浓度仍是1mol•L﹣1 |
|
| B. | 制成0.5L 10mol•L﹣1的盐酸,需标准状况下氯化氢气体112L |
|
| C. | 0.5L 2mol•L﹣1 BaCl2溶液中,Ba2+和Cl﹣总数为3×6.02×1023 |
|
| D. | 10g 98%硫酸(密度为1.84g•cm﹣3)与10mL 18.4 mol•L﹣1硫酸的浓度是不同的 |
考点:
物质的量浓度的相关计算.
专题:
物质的量浓度和溶解度专题.
分析:
A、根据溶液为均一、稳定的混合物来分析.
B、根据n=c•v和V=n•Vm来计算.
C、根据n=c•v和N=n•NA来计算.
D、据c=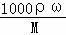 来计算.
来计算.
解答:
解:A、溶液为均一、稳定的混合物,从1L 1mol•L﹣1的NaCl溶液中取出10mL,浓度不变,浓度仍是1mol•L﹣1,故A正确.
B、制成0.5L 10mol•L﹣1的盐酸,需要n(HCl)=c•v=0.5L×10mol•L﹣1=5mol,标准状况下体积V(HCl)=n•Vm=5mol×22.4mol•L﹣1=112L,故B正确.
C、0.5L 2mol•L﹣1 BaCl2溶液中,n(BaCl2)=c•v=0.5L×2mol•L﹣1=1mol,由BaCl2的构成可知,1molBaCl2含3mol离子,即3×6.02×1023个,故C正确.
D、据c=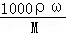 可知,98%硫酸(密度为1.84g•cm﹣3)的物质的量浓度c=
可知,98%硫酸(密度为1.84g•cm﹣3)的物质的量浓度c=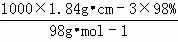 =18.4mol•L﹣1,与10mL 18.4 mol•L﹣1硫酸的浓度是相同的,故D错误.
=18.4mol•L﹣1,与10mL 18.4 mol•L﹣1硫酸的浓度是相同的,故D错误.
故选D.
点评:
本题考查的是物质的量浓度和离子数目的相关计算,注意物质的量公式的相关应用.


科目:高中化学 来源: 题型:
工业接触法制硫酸的简单流程图如下:
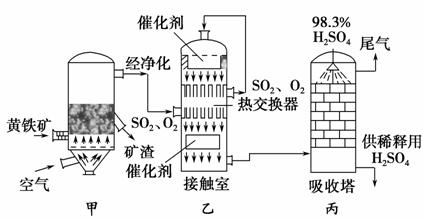
(1)写出装置甲的名称________。要使黄铁矿充分和迅速地燃烧,工业上常采取的措施为__________________________________。
(2)接触室中二氧化硫与氧气的反应采用________(填“常压”或“高压”),原因是____________________________________________________。
(3)刚通入接触室中的SO2和O2在热交换器的管道________(填“里”或“外”)流动,在催化剂表面接触反应的SO2和O2在热交换器的管道________(填“里”或“外”)流动,这样两种流体通过管壁进行热交换。
(4)在吸收塔中为什么用98.3%的浓硫酸而不是用水吸收三氧化硫?______________________________________________________________。
(5)工业接触法制硫酸的过程中,有两个操作过程采用了逆流的原理,它们分别是________________________________________________,
________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,反应SO2(g)+ O2(g)⇌SO3(g)的平衡常数K1=50,在同一温度下,反应2SO3(g)⇌2SO2(g)+O2(g)的平衡常数K2的值为( )
O2(g)⇌SO3(g)的平衡常数K1=50,在同一温度下,反应2SO3(g)⇌2SO2(g)+O2(g)的平衡常数K2的值为( )
|
| A. | 2500 | B. | 100 | C. | 4×10﹣4 | D. | 2×10﹣2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
为了除去KCl中的Ca2+,Mg2+,SO42﹣及泥沙,得到纯净的KCl,可将固体溶于水,然后在下列操作中选取必要的步骤和最佳的操作顺序( )
①过滤 ②加过量KOH溶液 ③加适量盐酸 ④加过量K2CO3溶液 ⑤加过量BaCl2溶液.
|
| A. | ②①⑤①④①③ | B. | ④①②⑤③ | C. | ②⑤④①③ | D. | ①④②⑤③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
两个体积相同的密闭容器一个盛氯化氢,另一个盛有H2和Cl2的混合气体,在同温同压下,两个容器内的气体一定具有相同的是( )
|
| A. | 质量 | B. | 密度 | C. | 电子总数 | D. | 原子总数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为 mol•L﹣1.
(2)取用任意体积的该盐酸溶液时,下列物理量中,不随取用的体积多少而变化的是 .
A.HCl的摩尔质量 B.溶液的浓度
C.溶液中Cl﹣的质量分数 D.溶液的密度
(3)某学生用上述浓盐酸和蒸馏水配制480mL 物质的量浓度为0.4mol•L﹣1的稀盐酸.
①该学生需选择容量瓶的规格为 mL;(填:100、250、500、1000)
该学生需要量取 ml 上述浓盐酸进行配制.
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?
Ⅰ.用量筒量取浓盐酸时,俯视观察凹液面
Ⅱ.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
(填:“偏大”、“偏小”或“无影响”).

查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生产、生活和社会密切相关.下列说法不正确的是()
A. 漂白粉长期暴露在空气中会变质失效
B. 雾霾天车灯照射的光亮通路属于丁达尔现象
C. 硬铝属于合金材料,瓷器属于硅酸盐制品
D. 不锈钢具有较强的抗腐蚀性,是因为在钢铁表面镀上了金属铬
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是一个一次性加热杯的示意图。当水袋破裂时,水与固体碎块混和,杯内食物温度逐渐上升。制造此加热杯可选用的固体碎块是( )
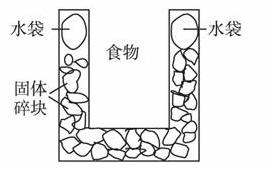
A.硝酸铵 B.生石灰 C.氯化镁 D.食盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com