
����Ŀ��ͭ�滭��һ���ư淽����������Ϳ�ڱ�ͭ�����������Ĥ���õ���ȥ����Ĥ������Ȼ�����FeCl3��ʴҺ�С���ȥĤ֮������ʴ���γɰ��ߡ�ӡˢʱ���߿ɴ���ī����ͭ���ֽѹ������ī����ֽ�ϣ��γɵ��š�ׯ�ص�ͭ�滭��

��1��д��FeCl3��ʴͭ������ӷ���ʽ___________________
��2�����д�ʩ���Լӿ�ͭ��ĸ�ʴ���ʵ���____________�����ţ�
A. ���� B. ���Ȼ�ͭ C. ������̼�� D. ������
��3��ͨ�������üӿ츯ʴ���ʵ�ԭ����_________________
��4����ȥ�������Ĥ��漴�γɡ�����________��ȥ����Ĥ�����ţ�
A. ����Na2CO3��Һ B. ú�� C. ��Һ D.��Һ
��5��ʵ�����ù����Ȼ�������FeCl3��Һ�ļ�����_____________
��6����ʴ��ķ�Һ�����ԣ��м���NaNO3������NO���壬д��������Ӧ�����ӷ���ʽ����ע������ת�Ƶķ������Ŀ��__________________________
��7��Ҫ��֤��ʴ��ķ�Һ�к���Fe3+��������Һ�м����Լ�_________������_______________
���𰸡� Cu+2Fe3+==Cu2++2Fe2+ AC ��Ӧ���ʹ��첻���ư��ߵ��������Ӷ�Ӱ��滭������ B �������Ȼ�������Ũ�����У��ټ�ˮϡ�� 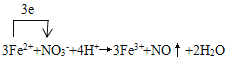 KSCN��Һ ��Һ��Ѫ��ɫ
KSCN��Һ ��Һ��Ѫ��ɫ
����������1���Ȼ������������ԣ����FeCl3��ʴͭ������ӷ���ʽΪCu+2Fe3+��Cu2++2Fe2+����2�� A. ������Ӧ���ʼӿ죬A��ȷ��B. ���Ȼ�ͭͭ����Ũ���������ڷ�Ӧ��B������C. ������̼����ͭ����ԭ��أ��ӿ췴Ӧ���ʣ�C��ȷ��D. ������ͭ����Ӧ��D��������ѡAC����3��������Ӧ���ʹ��첻���ư��ߵ��������Ӷ�Ӱ��滭�����������ͨ�������üӿ츯ʴ��������4�����������л�����Ӧ����ú���ܽ⣬��ѡB����5���Ȼ���ˮ�⣬����ʵ�����ù����Ȼ�������FeCl3��Һ�ļ����ǽ������Ȼ�������Ũ�����У��ټ�ˮϡ������6��������Һ��������ܰ�����������������������ԭΪNO����Ӧ�����ӷ���ʽΪ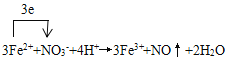 ����7��Ҫ��֤��ʴ��ķ�Һ�к���Fe3+��������Һ�м���KSCN��Һ����������Һ��Ѫ��ɫ��
����7��Ҫ��֤��ʴ��ķ�Һ�к���Fe3+��������Һ�м���KSCN��Һ����������Һ��Ѫ��ɫ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��þ��һ����Ҫ�Ľ�����Դ���ڸ���������Ҫ�����á�
��1��Ƥ������þ���ҹ�����þ����Ҫ��������ʵ�����ڸ��º���������£��������ƴ���ʱ��ͨ���軹ԭ����þ����þ�������뷴Ӧ���ɵĹ���������(2CaO��SiO2)����룬���������õ��ᾧþ��д���÷�Ӧ�Ļ�ѧ��Ӧ����ʽ ��
�������ȵõ�����þ��������þ�������������� (����)�����Χ����ȴ��
A������ B������ C��ˮ���� D������
��2��Ŀǰ�������80%��þ�����ڵ�������Ȼ�þ�����ԭ����ˮ�Ȼ�þ���ɺ�ˮ�Ʊ�����Ҫ�����²��裺���ڸ����HCl�����м�����ˮ���������ʯ�ң�������������ˣ���Ũ����ȴ�ᾧ��
�䲽���Ⱥ�˳����_____________________��������ظ�ʹ�ã����ڸ����HCl�����м���ʱ���ܵõ���ˮMgCl2����ԭ����______________________��
��3����֪ij�¶���Mg(OH)2��Ksp��6.4��l012������Һ��c(Mg2+)��1.0��105mol��L1����Ϊ������ȫ������¶���Ӧ������Һ��c(OH��)��_______________mol��L1��
��4����Mg(OH)2����Һ�е��뱥��NH4Cl��Һ����Һ���������Ӧԭ�������������һ��NH4+ˮ�����H+��H+����Mg(OH)2��Ӧ������_____________________�������ӷ���ʽ��ʾ����Ҫ��֤˭��Mg(OH)2�ܽ����Ҫԭ��ѡȡ________����NH4Cl��Һ������ʵ�顣
A��NH4NO3 B��(NH4)2SO4 C��CH3COONH4 D��NH4HCO3
��5��þ����ǽ�������ѧ�����о����ȵ�֮һ����ͼΪMg��NaClOȼ�ϵ�ؽṹʾ��ͼ���乤��ʱMg�� ���X����Y�����缫�������ĵ缫��Ӧʽ�� ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���ӵ����ģ������ͼ��ʾ����֪����������ԭ�ӵ��������ﵽ8�����ȶ��ṹ��ԭ�Ӽ��Ե��������������й�˵���д������( )
![]()
A. Xԭ�ӿ���Ϊ����A��Ԫ��
B. Yԭ��һ��Ϊ����A��Ԫ��
C. �÷����мȺ��м��Թ��ۼ��ֺ��зǼ��Թ��ۼ�
D. ��Բ��Ĵ�С�������÷��ӿ���ΪN2F4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯�����ڹ�ũҵ�����о�����Ҫ���á�
���������գ�

��1����ͼ��ʾΪԪ�����ڱ��е�Ԫ�ز�����Ϣ�����ݡ�14.01����ʾ����____________����ԭ������������________�ֲ�ͬ����������_______�ֲ�ͬ�˶�״̬��
��2��NH3�����������������Ϊ________________NH4Cl��Һ��NaOH��Һ��������ԣ���c��Na+��_______c��NH3H2O�����<��>����=����
��3��д��һ���ܱȽϵ���������Ԫ�طǽ�����ǿ������ʵ��________________
�о�NO2��SO2��CO�ȴ�����Ⱦ��Ĵ���������Ҫ���塣NO2�������з�Ӧ��������
![]()
��4��д��������Ӧ��ƽ�ⳣ������ʽ_______________����÷�Ӧƽ�ⳣ���Ĵ�ʩ��__________�����ţ�
A. ��ѹ B. ����NH3��Ũ�� C. ���� D. ��ʱ���߲���
��5��һ��������������Ӧ��ij����̶����ܱ������н��У���˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����__________�������ţ�
A. c(NO2) : c(NH3)=3:4 B. ![]()
![]()
C. ������������ѹǿ���ٱ仯 D. �����������ܶȲ��ٱ仯
��6��ij�¶��£���һ���ݻ�Ϊ2���ķ�Ӧ�����ڣ�������Ӧ2���Ӻ�ﵽƽ�⣬����NO2������0.75mol������2������NH3��ƽ����Ӧ����Ϊ�� ![]() =_____________
=_____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ᣨCH3COOOH����ǿ�����ԣ�����������桢Ƥ�������ߡ����������������Ʊ���ӦΪ��CH3COOH��H2O2![]() CH3COOOH��H2O�������й�˵����ȷ����
CH3COOOH��H2O�������й�˵����ȷ����
A. ����ѹǿ�ɼӿ�÷�Ӧ����
B. ������ʵĴ����ɸı�÷�Ӧ�ķ�Ӧ��
C. �ﵽƽ��ʱ����������ֱ�ʾ���淴Ӧ���ʶ���v(��)��v(��)
D. �ﵽƽ��ʱ��H2O2ת����Ϊ100%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������пƬ�ʹ�ͭƬ��ͼ��ʽ����ͬŨ�ȵ�ϡ������һ��ʱ�䣬����������ȷ����

A. ���ձ���ͭƬ����������ݲ���
B. ����ͭƬ������������ͭƬ�Ǹ���
C. ���ձ�����Һ��pH������
D. �ס�����Һ������ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڱ�(��ͼ��ʾ)��������ȷ���ǣ� ��

A. ��Ӧ�ڲ��������������зֲ�������ɫ�����²�
B. ��Ӧ�ٳ������ܽ��У����л�����Ϊ![]()
C. ��Ӧ��Ϊ�ӳɷ�Ӧ���������������ױ�
D. ��Ӧ����1mol�������3 mol H2�����ӳɷ�Ӧ������Ϊ�����Ӻ�������̼̼˫��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��4P������s��![]() P4������s�� ��H = +17kJmol��1�������Ϸ���ʽ������������ȷ����
P4������s�� ��H = +17kJmol��1�������Ϸ���ʽ������������ȷ����
A. ����Ӧ��һ�����ȷ�Ӧ
B. ��lmol������ȫת��ɺ���ʱ�ų�17kJ����
C. ��4g����ת��ɰ���ʱ����17kJ����
D. ���ױȺ����ȶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʯ�ͺ�ʯ�ͻ�����˵��������ǣ� ��
A. ʯ�͵���Ҫ�ɷ���̼�⻯����
B. ʯ�ͷ���õ��ĸ�������ǻ����
C. ʯ���ѽ�������Ҫ�ɷ��Ǽ���
D. ʯ���ѻ���Ŀ����Ϊ����������͵IJ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com