
| A. | 为防止电池中的重金属污染土壤和水体,应积极开发废旧电池的综合回收利用 | |
| B. | 氢能是清洁能源,工业上电解水法制大量氢气符合节能减排理念 | |
| C. | 大量的汽车尾气是造成雾霾天气的一个重要因素 | |
| D. | 煤的液化和气化均属于化学变化 |
分析 A、电池中的重金属离子会带来污染;
B、电解水消耗大量的能源;
C、汽车尾气中含SO2等气体和颗粒物;
D、没有新物质生成的变化是物理变化,有新物质生成的变化是化学变化.
解答 解:A、电池中的重金属离子会带来污染,为防止电池中的重金属离子污染土壤和水源,应积极开发废旧电池的综合利用技术,故A正确;
B、氢能是清洁能源,但电解水消耗大量的能源,电解水法制大量氢气不符合节能减排理念,故B错误;
C、汽车尾气释放出SO2等气体和颗粒物,是造成雾霾天气的重要因素之一,故C正确;
D、煤的气化是将其转化为可燃性气体的过程,属于化学变化;煤的液化是使煤与氢气作用生成液体燃料,属于化学变化,故D正确;
故选B.
点评 本题考查原电池对环境的污染、物理变化和雾霾的形成,明确物质的成分和性质即可解答,难度不大.


 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源:2016-2017学年甘肃省高二上10月月考化学试卷(解析版) 题型:选择题
下列盐的水溶液,其pH值小于7的是 ( )
A.NaHCO3溶液 B.NaCl溶液 C.Na2SO4溶液 D.NH4Cl溶液
查看答案和解析>>
科目:高中化学 来源:2017届重庆一中高三上学期第二次月考化学试卷(解析版) 题型:选择题
某羧酸酯的分子式为C57H104O6,1 mol该酯完全水解可得到3 mol羧酸M和1 mol甘油[HOCH2CH(OH)CH2OH]。羧酸M的分子式为( )
A.C17H32O2 B.C18H34O2 C.C18H36O2 D.C19H36O2
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
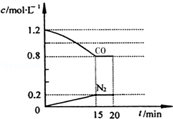 回答下列问题:
回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向容积固定的容器甲和带有活塞的定压容器乙中分别通入2mol SO2和1mol O2(如下图),若开始通气时两容器的体积相同,在相同温度下反应,一段时间后,反应达到平衡.则下列说法正确的是( )
向容积固定的容器甲和带有活塞的定压容器乙中分别通入2mol SO2和1mol O2(如下图),若开始通气时两容器的体积相同,在相同温度下反应,一段时间后,反应达到平衡.则下列说法正确的是( )| A. | 平衡时,两容器内SO3的浓度必定相等 | |
| B. | 平衡时,混合气体中的SO3的体积分数甲比乙高 | |
| C. | SO2的转化率乙容器内比甲容器内高 | |
| D. | 反应后的相同时间内,甲容器中的反应速率大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向盐酸中滴加氨水:H++OH-═H2O | |
| B. | 氯化钙与碳酸氢钾溶液混合:Ca2++CO32-═CaCO3↓ | |
| C. | 氢氧化铝中和胃酸:Al(OH)3+3H+═Al3++3H2O | |
| D. | Ca(HCO3)2溶液中加入过量KOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4NH3+5O2═4NO+6H2O | B. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||
| C. | 2NaHCO3═Na2CO3+H2O+CO2 | D. | Cl2+2NaBr═2NaCl+Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com