
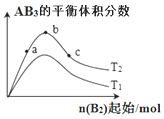
 某化学科研小组研究在其它条件不变时,改变某一条件对化学反应:A2(g)+3B2(g)?2AB3(g)的平衡状态的影响时,得到如图所示的变化关系(图中T表示温度,n表示物质的量).下列推论正确的是( )
某化学科研小组研究在其它条件不变时,改变某一条件对化学反应:A2(g)+3B2(g)?2AB3(g)的平衡状态的影响时,得到如图所示的变化关系(图中T表示温度,n表示物质的量).下列推论正确的是( )| A. | 反应速率a>b>c | |
| B. | 若T2>T1,则正反应一定是放热反应 | |
| C. | 达到平衡时,AB3的物质的量大小关系:c>b>a | |
| D. | 达到平衡时,A2转化率的大小关系:a>b>c |
分析 对于可逆反应来说,增大一种反应物的物质的量或浓度,有利于平衡向正反应方向移动,则另一种反应物的转化率增大,生成物的物质的量增多,反应速率增大;升高温度平衡向吸热方向移动,由此分析解答.
解答 解:A、根据图象可知,a、b、c各点中B的起始物质的量依次增大,则反应物的浓度依次增大,反应速率依次增大,故A错误;
B、若T2>T1,由图象可知温度升高生成物的物质的量增大,说明升高温度平衡向正反应分析移动,则正反应为吸热反应,故B错误;
C、对于可逆反应来说,增大一种反应物的物质的量或浓度,有利于平衡向正反应方向移动,生成物的物质的量增多,故C正确;
D、根据图象可知,a、b、c各点中B的起始物质的量依次增大,对于可逆反应来说,增大一种反应物的物质的量或浓度,有利于平衡向正反应方向移动,则另一种反应物的转化率增大,则达到平衡时A2的转化率大小为:a<b<c,故D错误;
故选C.
点评 本题考查化学平衡移动图象题,题目难度不大,本题注意浓度对化学反应速率和化学平衡移动的影响.


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:推断题
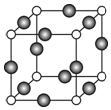 已知X、Y、Z、W、K五种元素均位于周期表的前四周期,且原子序数依次增大.元素X是周期表中原子半径最小的元素;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;W位于第2周期,其原子的核外成对电子数是未成对电子数的3倍;K位于ds区且原子的最外层电子数与X的相同.
已知X、Y、Z、W、K五种元素均位于周期表的前四周期,且原子序数依次增大.元素X是周期表中原子半径最小的元素;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;W位于第2周期,其原子的核外成对电子数是未成对电子数的3倍;K位于ds区且原子的最外层电子数与X的相同.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
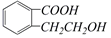 的有机物可以通过不同的反应得到下列四种物质:
的有机物可以通过不同的反应得到下列四种物质:
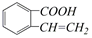

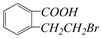
| A. | 取代、消去、酯化、加成 | B. | 取代、消去、加聚、取代 | ||
| C. | 酯化、取代、缩聚、取代 | D. | 酯化、消去、氧化、取代 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
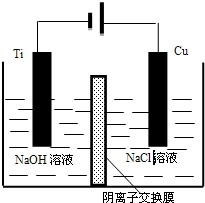 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:| 方法I | 用碳粉在高温条件下还原CuO |
| 方法II | 用肼(N2H4)还原新制Cu(OH)2 |
| 方法III | 电解法,反应为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑ |
| 序号 | Cu2O a克 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | 方法II | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | 方法III | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | 方法III | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
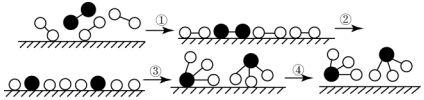
| A. | 该过程表明,在化学反应中存在化学键的断裂与形成 | |
| B. | 在催化剂的作用下,反应物的化学键变得容易断裂 | |
| C. | 过程②需吸收能量,过程③则放出能量 | |
| D. | 常温下该反应难以进行,是因为常温下生成物的化学键难以形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “歼-20”飞机上大量使用的碳纤维是一种新型的有机高分子材料 | |
| B. | “神舟十一号”宇宙飞船返回舱外表面主要是耐高温的新型无机非金属材料 | |
| C. | “天宮一号”是中国第一个空间实验室,其太阳能电池板的主要材料是二氧化硅 | |
| D. | “辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com