
| A. | ③④ | B. | ②③④ | C. | ①③④ | D. | 全部 |
分析 中学常见既能与NaOH溶液反应,又能与盐酸反应,又的物质有:铝、两性氧化物、两性氢氧化物、弱酸酸式盐、弱酸的铵盐、蛋白质、氨基酸等.
解答 解:①NaHCO3是弱酸酸式盐,与氢氧化钠反应得到碳酸钠,与盐酸反应得到氯化钠、二氧化碳与水,故①正确;
②Al2O3 是两性氧化物,与氢氧化钠反应得到偏铝酸钠,与盐酸反应得到氯化铝,故②正确;
③Al(OH)3 是两性氧化物,与氢氧化钠反应得到偏铝酸钠,与盐酸反应得到氯化铝,故③正确;
④Al属于两性金属,与氢氧化钠反应得到偏铝酸钠与氢气,与盐酸反应生成氯化铝与氢气,故④正确,
故选D.
点评 本题考查了物质的性质,难度不大,明确物质的性质是解本题的关键,注意归纳总结既能与酸又能与碱反应的物质.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 20mL 3mol/L 的X溶液 | B. | 20mL 2mol/L 的X溶液 | ||
| C. | 10mL 4mol/L的X溶液 | D. | 10mL 2mol/L的X溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaClO属于共价化合物 | |
| B. | ClO-与Ca2+、Fe2+、Al3+ 能大量共存 | |
| C. | 1L 0.1mol?L-1NaClO溶液中ClO-的数目为0.1NA | |
| D. | “84”消毒液在空气中久置变质发生了氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳分子的结构式:O-C-O | |
| B. | 氢氧根离子的电子式: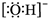 | |
| C. | 氯原子的结构示意图: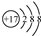 | |
| D. | 中子数为146、质子数为92 的铀(U)原子${\;}_{92}^{146}$U |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图表示的是在800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,请回答:
如图表示的是在800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
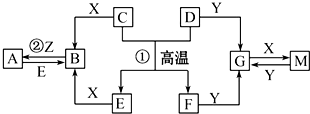
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为: N2(g)+3H2(g) $?_{500℃、30MPa}^{催化剂}$ 2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 | |
| D. | 1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者放出的热量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | FeCl3溶液中的Cl- | B. | Na2CO3溶液中的CO32- | ||
| C. | 氯化钡溶液中的Ba2+ | D. | 氟化钠溶液中的F- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com