
(1)在中和热的测定实验中,取50 mL 0.50 mol /L的盐酸,需加入下列 试剂(填序号)。①50 mL0.50 mol/L NaOH溶液 ②50 mL0.55 mol/L NaOH溶液③1.0 g NaOH固体
(2)在硫酸铜晶体结晶水含量的测定实验中,若坩埚的质量为m,坩埚与硫酸铜晶体的质量为m1,加热后称量坩埚与无水硫酸铜的质量为m2,则晶体中结晶水的质量分数ω=____________________(写计算式)。如果实验中加热温度过高,固体颜色变黑,则测定结果会____________(填“不变”、“偏高”、“偏低”)。
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源:北京市西城区2005年抽样测试、高三化学试卷 题型:022
在中和热的测定实验中,取50 mL 0.50 mol /L的盐酸,需加入下列________试剂(填序号).①50 mL0.50 mol/L NaOH溶液 ②50 mL0.55 mol/L NaOH溶液 ③1.0 g NaOH固体
查看答案和解析>>
科目:高中化学 来源:福建省长乐二中2006-2007学年上学期期中考试、高三化学试题 题型:022
(1)图Ⅰ表示10mL量筒中液面的位置,A与B刻度间相差1mL,如果刻度A为4,量筒中液体的体积是________mL.
(2)图Ⅱ表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)________.
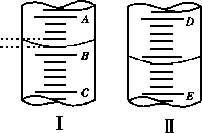
A、是amL
B、是(50-a)mL
C、一定大于amL
D、一定大于(50-a)mL
(3)能选用CCl4从碘水中萃取碘的原因是________.
(4)在中和热的测定实验中,取50mL0.50mol/L的盐酸,需加入下列________试剂(填序号).
①50mL0.50mol/LNaOH溶液②50mL0.55mol/LNaOH溶液③1.0gNaOH固体
(5)在硫酸铜晶体结晶水含量的测定实验中,若坩埚的质量为m,坩埚与硫酸铜晶体的质量为m1,加热后称量坩埚与无水硫酸铜的质量为m2,则晶体中结晶水的质量分数ω=________(写计算式).
查看答案和解析>>
科目:高中化学 来源:甘肃省张掖中学2007届高三年级模拟训练、化学试卷 题型:043
| |||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山西省高考一轮复习阶段考试化学试卷(解析版) 题型:实验题
(1)在中和热的测定实验中,取50 mL 0.50 mol /L的盐酸,需加入下列 试剂(填序号)。①50 mL0.50 mol/L NaOH溶液 ②50 mL0.55 mol/L NaOH溶液 ③1.0 g NaOH固体
 (2)在硫酸铜晶体结晶水含量的测定实验中,若坩埚的质量为m,坩埚与硫酸铜晶体的质量为m1,加热后称量坩埚与无水硫酸铜的质量为m2,则晶体中结晶水的质量分数ω=____________________(写计算式)。如果实验中加热温度过高,固体颜色变黑,则测定结果会____________(填“不变”、“偏高”、“偏低”)。
(2)在硫酸铜晶体结晶水含量的测定实验中,若坩埚的质量为m,坩埚与硫酸铜晶体的质量为m1,加热后称量坩埚与无水硫酸铜的质量为m2,则晶体中结晶水的质量分数ω=____________________(写计算式)。如果实验中加热温度过高,固体颜色变黑,则测定结果会____________(填“不变”、“偏高”、“偏低”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com