
| ������ | Al��OH��3 | Fe��OH��3 | Fe��OH��2 | Ni��OH��2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
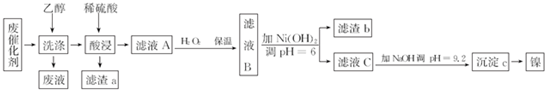
���� ���Ҵ�ϴ���ܽⲢ��ȥ�л������ʣ��������ʱ��Ҫ���ܽ�������������Al���ʣ�ֻ��SiO2�������ᷴӦ�����˵õ�����a��SiO2����ҺA����H2O2��Ŀ���ǽ�Fe2+����ΪFe3+��B��Һ����pH=6��ʹ��Һ��Fe3+��Al3+ת��Ϊ������������������������ͨ�����˶���ȥ���ɱ������ݣ������Լ�X��Ŀ���ǽ���ת��ΪNi��OH��2����X�Ǽ������ʣ�Ni��OH��2ת��Ϊ�������ķ������Ƚ������ʹ��ת��ΪNiO��Ȼ���û�ԭ�����л�ԭ����ͨ�����ȷ�Ӧ��
��1�����Ҵ�ϴ�ӵ�Ŀ�����ܽⲢ��ȥ�л������ʣ���������ķ����ɽ��Ҵ��������л�����뿪��ֻ��SiO2�������ᷴӦ��������a�ijɷ���SiO2��
��2�����ϴ���������ʵ�����������Ũ�ȡ�����ʱ���¶Ⱦ������������ʣ�
��3������H2O2��Ŀ���ǽ�Fe2+����ΪFe3+���ɱ������ݼ�����ͼ֪�������Լ�X��Ŀ���ǽ���ת��ΪNi��OH��2��
��4������Դ���ķ��������ѧ�Ƶ��ŵ㣻
��5��������Һ�õ�����IJ���Ϊ�����ᾧ��
�ڲ�Ʒ��������ʱ����������̷���FeSO4•7H2O������������������������H2O2���������㣨��H2O2ʧЧ�������ܻᵼ��Fe2+δ����ȫ�������Ӷ�ʹ��Ʒ�����л��������̷���FeSO4•7H2O����
��NiSO4��ǿ����Һ����NaClO���������Ƶü������ӵ�ص缫����--NiOOH���÷�Ӧ�����ӷ���ʽ�ǣ�2Ni2++ClO-+4OH-�T2NiOOH��+Cl-+H2O��
��� �⣺��1�����Ҵ�ϴ�ӵ�Ŀ�����ܽⲢ��ȥ�л������ʣ���������ķ����ɽ��Ҵ��������л�����뿪��ֻ��SiO2�������ᷴӦ��������a�ijɷ���SiO2���ʴ�Ϊ��SiO2���ܽ⡢��ȥ�л������
��2�����ϴ���������ʵ�����������Ũ�ȡ�����ʱ���¶Ⱦ������������ʣ��ʴ�Ϊ�����ϴ���������ʵ�����������Ũ�ȡ�����ʱ���¶ȣ�
��3�����ݷ�����֪��ҺA�п��ܺ��еĽ���������Al3+��Fe2+��Ni2+������H2O2��Ŀ���ǽ�Fe2+����ΪFe3+�������ڷ��룬��Ӧ���ӷ���ʽΪ��2Fe2++2H++H2O2=2Fe3++2H2O���ɱ������ݼ�����ͼ֪�������Լ�X��Ŀ���ǽ���ת��ΪNi��OH��2����X�Ǽ������ʣ�X����ΪNaOH��
�ʴ�Ϊ��Al3+��Fe2+��Ni2+������H2O2��Ŀ���ǽ�Fe2+����ΪFe3+�������ڷ��룻2Fe2++2H++H2O2=2Fe3++2H2O��
��4��������ȣ���ѧ�Ƶ�����ŵ��ǣ������ĵ��ܣ���Լ��Դ���ʴ�Ϊ�������ĵ��ܣ���Լ��Դ��
��5��������Һ�õ�����IJ���Ϊ�����ᾧ�����Բ���X�������������ᾧ���ʴ�Ϊ�������ᾧ��
�ڲ�Ʒ��������ʱ����������̷���FeSO4•7H2O������������������������H2O2���������㣨��H2O2ʧЧ�������ܻᵼ��Fe2+δ����ȫ�������Ӷ�ʹ��Ʒ�����л��������̷���FeSO4•7H2O�����ʴ�Ϊ��H2O2���������㣨��H2O2ʧЧ����
��NiSO4��ǿ����Һ����NaClO���������Ƶü������ӵ�ص缫����--NiOOH���÷�Ӧ�����ӷ���ʽ�ǣ�2Ni2++ClO-+4OH-�T2NiOOH��+Cl-+H2O���ʴ�Ϊ��2Ni2++ClO-+4OH-�T2NiOOH��+Cl-+H2O��
���� �����Թ�������Ϊ���壬���������ʷ����ᴿ����ѧ��Ӧ����Ӱ�����ء�����ת������ѧ���㡢������ԭ��Ӧ��ƽ�ȣ��Ǹ߿��������ͣ��ۺ��Խ�ǿ���漰֪ʶ��Ϲ㣬���ؿ���ѧ����֪ʶ��Ǩ��Ӧ�ã��ؼ��ǶԹ�����������������Ѷ��еȣ�


 ��ʦָ��һ��ͨϵ�д�
��ʦָ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��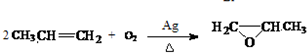 ��
�� ��
�� ��
��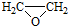 ����д�����ڼ����� ��
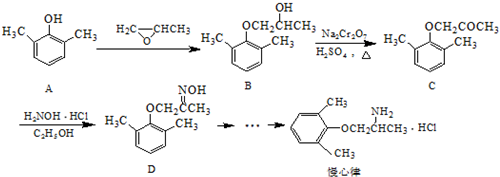
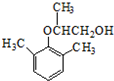
����д�����ڼ����� ��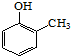 �����Ҵ�Ϊԭ���Ʊ�
�����Ҵ�Ϊԭ���Ʊ� 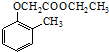 �ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�CH3CH2OH$��_{170��}^{ŨH_{2}SO_{4}}$CH2=CH2��
�ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�CH3CH2OH$��_{170��}^{ŨH_{2}SO_{4}}$CH2=CH2���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
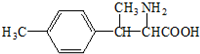
| A�� | 1-��ϩ��2-��-1-��ϩ | B�� | ��ȩ�ͼ������ | ||
| C�� | 1-�����ͼ����� | D�� | ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
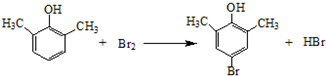
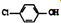 �������Է�ˮ�������������ط���ȥ����ԭ����ͼ2��ʾ
�������Է�ˮ�������������ط���ȥ����ԭ����ͼ2��ʾ -OH+2e-+H+�T
-OH+2e-+H+�T -OH+Cl-
-OH+Cl-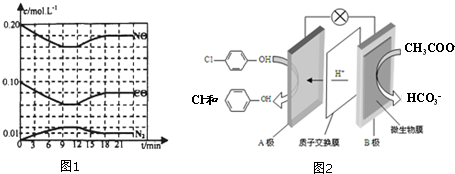
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ����� | ʵ��Ŀ�Ļ���� |
| A | ��0.1mol•L-1 Na2CO3��Һ����BaCl2��Һ�������г����������ٵμ�0.1mol•L-1 Na2SO4��Һ������������ | ֤��Ksp��BaSO4���� Ksp��BaCO3�� |
| B | ��ʢ��KI3��Һ�����Թ��зֱ���������Һ��AgNO3��Һ��ǰ����Һ����ɫ�������л�ɫ���� | ֤��KI3��Һ�д���I3-?I2+I-ƽ�� |
| C | ��NaAlO2��Һ�г���ͨ������Y���ȳ��ְ�ɫ���������ճ������ܽ� | Y������CO2���� |
| D | �������ữ��H2O2��Һ����Fe��NO3��2��Һ�У���Һ���ɫ | ֤�������ԣ�H2O2��Fe3+ǿ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1�� | B�� | 2�� | C�� | 3�� | D�� | 4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
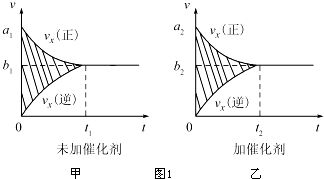
| �¶�/�� | 800 | 1000 | 1200 | 1400 |
| ƽ�ⳣ�� | 0.45 | 1.92 | 276.5 | 1771.5 |
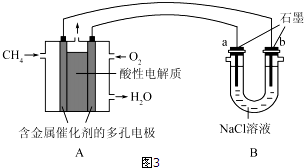
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ����Fe2O3�������ȷ�Ӧ����������������� | |
| B�� | Na��Al��Cu���Էֱ��õ��ұ�������Ȼ�ԭ�����ȷֽⷨ�õ� | |
| C�� | ������ͭ��Ũ���ᷴӦ������NO | |
| D�� | ������Ԫ�غ���Ԫ�ض���+3�ۣ���2Al+6HCl2�TAlCl3+3H2����֪��2Fe+6HCl2�TFeCl3+3H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
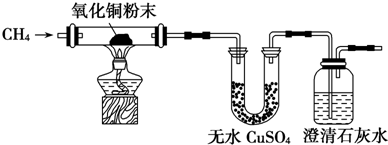
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com