
短周期中三元素a、b、c在周期表中的位置如图,下列有关这三种元素的叙述正确的是( )
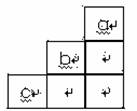
A.a是一种活泼的非金属元素
B.c的最高价氧化物的水化物是一种弱酸
C.b的氢化物很稳定
D.b元素的最高化合物为+7价。
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能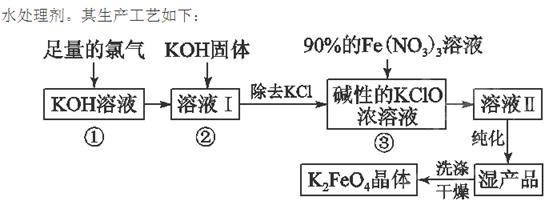 (1)反应①应在温度较低的情况下进行。因在温度较高时KOH与Cl2反应生成的是KClO3。写出在温度较高时KOH与Cl2反应的化学方程式 ,该反应的氧化产物是 。
(1)反应①应在温度较低的情况下进行。因在温度较高时KOH与Cl2反应生成的是KClO3。写出在温度较高时KOH与Cl2反应的化学方程式 ,该反应的氧化产物是 。
(2)在溶液Ⅰ中加入KOH固体的目的是 (填编号)。
A.与溶液Ⅰ中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO3转化为KClO
(3)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为 。
(4)如何判断K2FeO4晶体已经洗涤干净 。
(5)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:
___FeO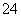 +____H2O — ____Fe(OH)3(胶体)+____O2↑+____OH-。
+____H2O — ____Fe(OH)3(胶体)+____O2↑+____OH-。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组反应(表内物质均为反应物)刚开始时,放出H2速率最大的是
| 编号 | 金属(粉末状) | 物质的量 | 酸的浓度 | 酸的体积 | 反应温度 |
| A | Al | 0.1 mol | 18.4 mol/L H2SO4 | 10 mL | 60 ℃ |
| B | Mg | 0.1 mol | 3 mol/L HCl | 10 mL | 30 ℃ |
| C | Fe | 0.1 mol | 3 mol/L H2SO4 | 10 mL | 60 ℃ |
| D | Mg | 0.1 mol | 3 mol/L H2SO4 | 10 mL | 60 ℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关原子结构和元素周期律表述正确的是( )
①原子序数为15的元素的最高化合价为+3
②ⅦA族元素是同周期中非金属性最强的元素
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为12的元素位于元素周期表的第三周期ⅡA族
A.①② B.①③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
丙烯酸的结构简式为CH2=CH—COOH,其对应的性质中不正确的是( )
A.与钠反应放出氢气 B.与新制的Cu(OH)2悬浊液反应
C.能与溴水发生取代反应 D.发生相互加成反应生成高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求用合适的化学用语填空
在原子序数1—18号元素中:
(1)与水反应最剧烈的金属是_____________。
(2)与水反应最剧烈的非金属单质是_____________。
(3)原子半径最小的元素是_____________。
(4)气态氢化物最稳定的化学式是_____________。
(5)最高价氧化物对应水化物的酸性最强的化学式是_____________。
(6)电子数为10的分子(写5个)
查看答案和解析>>
科目:高中化学 来源: 题型:
从不同的角度,化合物可分为不同的类别。下列共有12种有机化合物,请你设想一个分类依据,将它们分为不同的类别,将序号填入下表。

| 分类依据 | 有机化合物序号 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表短周期的一部分
| ① | ||||||||
| ② | ③ | ④ | ||||||
| ⑤ | ⑥ | ⑦ |
(1)①—⑦元素中金属性最强的元素位于周期表第 ▲ 周期 ▲ 族。
(2)可作为半导体材料的是 ▲ (写元素符号)。
(3)表中元素⑥的原子结构示意图为 ▲ 。
(4)④与⑤形成的常见化合物的化学键的类型为 ▲ ,该化合物的电子式为 ▲ 。
(5)表中元素①、②、③、⑤、⑦中,原子半径由大到小的顺序是 ▲ (填数字序号)
(6)表中元素③、⑥它们最高价氧化物的水化物相互反应的离子方程式为 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com