
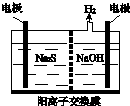
 Ⅰ硫化氢的转化是资源利用和环境保护的重要研究课题.由硫化氢获得硫单质有多种方法.
Ⅰ硫化氢的转化是资源利用和环境保护的重要研究课题.由硫化氢获得硫单质有多种方法.

科目:高中化学 来源: 题型:
| A、135 |
| B、64g?mol-1 |
| C、64 |
| D、135g?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、刚充入时反应速率v(正)增大,v(逆)增大 |
| B、达到新的平衡时,反应混合物中A、B的体积分数减小 |
| C、充入A、B、Q后,体系压强先增大,后逐渐减小 |
| D、若B为有色物质,达到新平衡后混合气颜色比原平衡浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶解 |
| ① |
| BaCl2 |
| ② |
| NaOH |
| ③ |
| Na2CO3 |
| ④ |
| 过滤 |
| ⑤ |
| 适量盐酸 |
| ⑥ |
| 蒸发、结晶、烘干 |
| ⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝和氢氧化钠反应 |
| B、氯化铝溶液中滴加足量氢氧化钠溶液 |
| C、向NaAlO2溶液中通入过量的CO2气体 |
| D、氯化铝溶液中滴加足量的氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、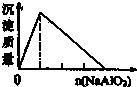 盐酸中加入NaAlO2溶液 |
B、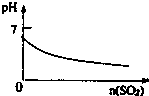 SO2气体通入溴水中 |
C、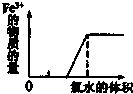 在FeBr2溶液中滴加氯水 |
D、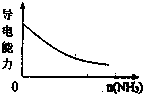 氨气通入醋酸溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com