
| A. | SO42-的空间构型是正四面体形 | |
| B. | CS2分子中各原子均达8电子稳定结构 | |
| C. | CH3-CH=CH2分子中碳原子的杂化类型有sp2和sp3两种 | |
| D. | H2O2分子是只含极性键的非极性分子 |
分析 A.SO42-中价层电子对个数是4且不含孤电子对,空间构型是正四面体形;
B.ABn型分子,A的族序数+成键数=8,则满足所有原子均达到8e-稳定结构;
C.甲基中的C原子为sp3杂化,C=C中的C原子为sp2杂化;
D.H202氧原子和氧原子之间形成的是非极性共价键,氢原子和氧原子之间形成的是极性共价键,H202正负电荷重心不重合,为极性分子;
解答 解:A.根据价层电子对互斥理论,价层电子对个数=σ键+孤电子对个数,SO42-中中心原子S的价层电子对为$\frac{6+2}{2}$=4,孤电子对数为$\frac{6+2-2×4}{2}$=0,不含孤电子对,所以空间构型是正四面体结构,故A正确;
B.CS2A的族序数+成键数=8(4+4=8),分子中各原子均达到8e-稳定结构,故B正确;
C.甲基中的C为sp3杂化,双键上C为sp2杂化,则有机物CH2=CH-CH3中甲基1个碳原子是sp3杂化,其余2个碳原子是sp2杂化,故C正确;
D.H202是共价化合物,氢原子与氧原子之间形成的是极性共价键,氧原子和氧原子之间形成的是非极性共价键,该分子正负电荷重心不重合,为极性分子,故D错误;
故选D.
点评 本题考查较综合,涉及原子杂化方式的判断、空间构型、分子极性、化学键等,为高考频点,注意根据价层电子对互斥理论来分析,题目难度中等.


 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| X | SO2 | Cl2 | HCl | NO2 |
| Y | NaHCO3 溶液 | 饱和Na2SO3溶液 | 饱和NaCl溶液 | 水 |
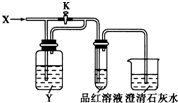
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
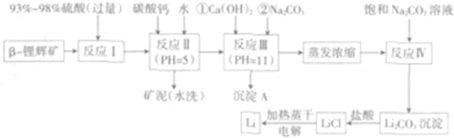
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
| 温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 原子序数 | 电子排布式 | 价层电子排布 | 周期 | 族 |
| 8 | 1s22s22p4 | 2s22p4 | 第二周期 | ⅥA |
| 24 | 1s22s22p63s23p63d54s1 | 3d54s1 | 第四周期 | ⅥB |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液质量减轻 | |
| B. | Fe3+的氧化性大于Cu2+ | |
| C. | 溶液中Cu2+与Fe2+的物质的量比为1:1 | |
| D. | Fe位于元素周期表第四周期Ⅷ族,是一种过渡金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
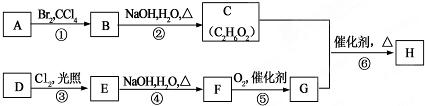
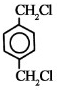 ;
;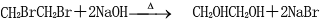 ⑥
⑥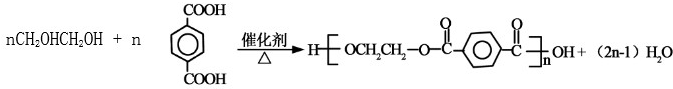 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图中的实验装置可用于制取乙炔.请填空:
如图中的实验装置可用于制取乙炔.请填空:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com