
【题目】下列不是反应速率限制外因的是( )
A.温度B.物质的性质C.浓度D.催化剂
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】根据反应Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,回答下列问题:
CuSO4+SO2↑+2H2O,回答下列问题:
(1)用“双线桥法”标出电子转移的方向和数目________________。
(2)请用化学式写出该反应中的还原剂是__________;氧化剂是__________;氧化产物是__________。
(3)还原剂和还原产物物质的量之比__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以芳香烃A(C7H8)为主要原料合成重要的医药中间体J的流程图如下:
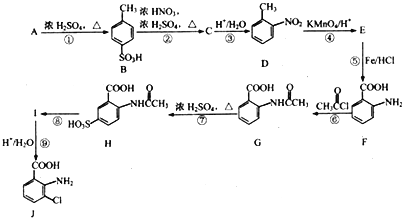
己知:①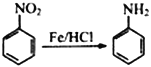 (-NH2易于被强氧化剂氧化)
(-NH2易于被强氧化剂氧化)
②![]()
③![]()
回答下列问题:
(1)A的结构简式为__________,其分子中不同化学环境的氢原子的个数比为__________。
(2)B→C 的化学方程式为_____________________,反应④的反应类型为__________。
(3)反应⑧所需试剂和条件为___________;E中含氧官能团的名称为_____________。
(4)反应⑥和⑦的顺序是否可以交换过来?__________(选填“是”或“否”)。分析⑥→⑨步的反应,其中反应⑥的主要目的是_____________________。
(5)K是J的同分异构体,其苯环上的取代基与J的相同但位置不同,则K可能的结构有__________种。
(6)请参照题中所示合成路线,以苯和![]() 为原料(无机试剂任选),设计制备
为原料(无机试剂任选),设计制备![]() 的合成路线__________。合成路线示例如下:CH3CH2OH
的合成路线__________。合成路线示例如下:CH3CH2OH![]() CH2=CH2
CH2=CH2![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2molA和1molB,发生反应:2A(g)+B(g)![]() 2D(g)△H=QkJ/mol。相关条件和数据见下表:
2D(g)△H=QkJ/mol。相关条件和数据见下表:
实验编号 | 实验I | 实验II | 实验III |
反应温度/℃ | 700 | 700 | 750 |
达平衡时间/min | 40 | 50 | 30 |
n(D)平衡/mol | 1.5 | 1.5 | 1 |
化学平衡常数 | K1 | K2 | K3 |
下列说法正确的是
A. 升高温度能加快反应速率的原理是降低了反应的活化能,使活化分子百分数提高
B. 实验III达平衡后,保持其他条件不变,再向容器中通入1molA和1molD,平衡不移动
C. 实验III达平衡后容器内的压强是实验1的9/10倍
D. K3>K2>K1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300 ℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)![]() 2 C(g)+2D(g) ΔH=Q, 2 min末达到平衡,生成0.8 mol D。
2 C(g)+2D(g) ΔH=Q, 2 min末达到平衡,生成0.8 mol D。
(1)300℃时,该反应的平衡常数表达式为K=______________,已知K300℃<K350℃,则ΔH____0(填“>”或“<”)。
(2)在2 min末时,B的平衡浓度为________,D的平均反应速率为________。
(3)若温度不变,缩小容器容积,则A的转化率________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I(化学反应原理)
(1)25℃,100 mL氢氧化钡溶液中含有1×10-3 mol的OH-,该溶液的pH为_________。
(2)常温下,CuCl2的水溶液呈_____(填“酸”、“中”或“碱”)性,原因是_______________(用离子方程式表示)。
(3)把AlCl3溶液在空气中蒸干、灼烧,最后得到的主要固体产物是_________。
(4)等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液中
c(Na+)________c(CH3COO-)(填“ >”、“=”或“<” )。
II(化学与生活)
有四种常见药物 ①阿司匹林 ②青霉素 ③胃舒平 ④麻黄碱.请回答:
(1)某同学胃酸过多,应选用的药物是______(填序号),抗酸药是治疗胃酸过多的一类药品,请写出一种抗酸药(有效成分是碳酸钙)中和胃酸过多的化学反应方程式:___________________________。
(2)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是_________(填序号)。
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是_______(填序号)。
(4)滥用药物会导致不良后果,如过量服用________(填序号)会出现水杨酸中毒,应立即停药,并静脉注射___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲配制80 g质量分数为10%的氢氧化钠溶液,如图是配制该氢氧化钠溶液的实验操作示意图。
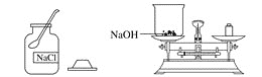
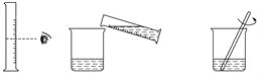
实验步骤
(1)计算:需要氢氧化钠固体__________g,水__________mL(水的密度为1 g·mL-1)。
(2)称量:用托盘天平称取氢氧化钠固体,用规格为__________(填“10mL”“50mL”或“100mL”)的量筒量取所需要的水,倒入盛有氢氧化钠的烧杯中。
(3)溶解:用玻璃棒搅拌,使氢氧化钠固体完全溶解。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个等体积的恒容密闭容器中,反应2CO2(g)+6H2(g) ![]() C2H5OH(g)+3H2O(g)达平衡,下列说法正确的是
C2H5OH(g)+3H2O(g)达平衡,下列说法正确的是
容器 | 温度/K | 物质的起始浓度(mol/L) | 物质的平衡浓度(mol/L) | |||
CO2(g) | H2(g) | C2H5OH(g) | H2O(g) | C2H5OH(g) | ||
甲 | 500 | 0.20 | 0.60 | 0 | 0 | 0.083 |
乙 | 500 | 0.40 | 1.20 | 0 | 0 | |
丙 | 600 | 0 | 0 | 0.10 | 0.30 | 0.039 |
A. 该反应正反应为吸热反应
B. 达平衡时,容器甲中的逆反应速率比容器乙中的小
C. 达平衡时,转化率:α(CO2 ,甲)+α(C2H5OH ,丙)>1
D. 达平衡时,甲、乙容器内:2c(CO2 ,甲)<c(CO2 ,乙)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com