
���� ��1�����뵪����Ӧ����Si3N4��
��2������֪����.3Si��s��+2N2��g��=Si3N4��s����H=-750.2kJ/mol
��Si��s��+2Cl2��g��=SiCl4��g����H=-609.6kJ/mol
��.$\frac{1}{2}$H2��g��+$\frac{1}{2}$Cl2��g��=HCl��g����H=-92.3kJ/mol
���ݸ�˹���ɣ���-���3+���12�ɵã�3SiCl4��g��+2N2��g��+6H2��g��=Si3N4��g��+12HCl��g������Ӧ��Ҳ������Ӧ�ļ��㣻
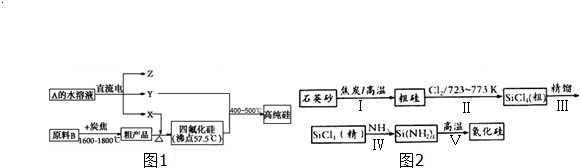
��ԭ��B��̼�õ��ֲ�Ʒ��X��Ӧ����SiCl4����XΪ������ԭ��B��̼�õ��ֲ�ƷΪSi����BΪSiO2��Y�������ڹ��ջ��ȼ�����¿ɷ�Ӧ������SiCl4��Ӧ�õ��ߴ���Si����YΪ������Z����ɫ�ʻ�ɫ������NaԪ�أ����A�õ�������������Z����ZΪNaOH��AΪNaCl��
��3���ٶ����������������Ʒ�Ӧ���ɹ�������ˮ��
�ڷ�Ӧ��Ϊ�û���Ӧ����Ӧ��Ϊ�е��ʲμӵĻ��Ϸ�Ӧ����������δ�����仯������Ԫ�ػ������Ϊ�����仯��
��SiCl4ˮ��õ�HCl��H2SiO3��
���ڷ�ӦIV�����Ȼ����백����Ӧ����Si��NH2��4��һ�����壬��Ԫ���غ��֪��������ΪHCl���ڷ�ӦV��Si��NH2��4���ȷֽ�����Si3N4����ԭ���غ��֪��һ�ֲ���ΪNH3��
��� �⣺��1�����뵪����Ӧ����Si3N4����Ӧ����ʽΪ��3Si+2N2$\frac{\underline{\;1300��1400��\;}}{\;}$Si3N4��
�ʴ�Ϊ��3Si+2N2$\frac{\underline{\;1300��1400��\;}}{\;}$Si3N4��
��2������֪����.3Si��s��+2N2��g��=Si3N4��s����H=-750.2kJ/mol
��Si��s��+2Cl2��g��=SiCl4��g����H=-609.6kJ/mol
��.$\frac{1}{2}$H2��g��+$\frac{1}{2}$Cl2��g��=HCl��g����H=-92.3kJ/mol
���ݸ�˹���ɣ���-���3+���12�ɵã�3SiCl4��g��+2N2��g��+6H2��g��=Si3N4��g��+12HCl��g�����ʡ�H=-750.2kJ/mol-3����-609.6kJ/mol��+12����-92.3kJ/mol��=-29.0kJ/mol��
�ʴ�Ϊ��3SiCl4��g��+2N2��g��+6H2��g��=Si3N4��g��+12HCl��g����H=-29.0kJ/mol��
��ԭ��B��̼�õ��ֲ�Ʒ��X��Ӧ������SiCl4����XΪ������ԭ��B��̼�õ��ֲ�ƷΪSi����BΪSiO2��Y�������ڹ��ջ��ȼ�����¿ɷ�Ӧ������SiCl4��Ӧ�õ��ߴ���Si����YΪ������Z����ɫ�ʻ�ɫ������NaԪ�أ����A�õ�������������Z����ZΪNaOH��AΪNaCl��
�������������е��NaCl��ˮ��Һʱ�����������ӷŵ���������������������ΪCu����Cu�ŵ磬�����Ӳ��ܷŵ��������������������ϲ���ΪCu��
CuΪ�������NaCl��ˮ��Һ��ʼһ��ʱ�䣬����Cu�ŵ�����ͭ���ӣ������缫��ӦʽΪ��Cu-2e-=Cu2+��
����ˮ�ŵ��������������������ӣ������缫��ӦʽΪ��2H2O+2e-=H2��+2OH-��
�ʴ�Ϊ�����ܣ�Cu-2e-=Cu2+��2H2O+2e-=H2��+2OH-��
��3���ٶ����������������Ʒ�Ӧ���ɹ�������ˮ����Ӧ����ʽΪ��SiO2+2NaOH=Na2SiO3+H2O��
�ʴ�Ϊ��SiO2+2NaOH=Na2SiO3+H2O��
�ڷ�Ӧ��Ϊ�û���Ӧ����Ӧ��Ϊ�е��ʲμӵĻ��Ϸ�Ӧ�����߾�����������ԭ��Ӧ����������δ�����仯��δ������ѧ�仯������Ԫ�ػ������Ϊ�����仯�����ڷ�������ԭ��Ӧ��
�ʴ�Ϊ��I����
��SiCl4ˮ��õ�HCl��H2SiO3����Ӧ����ʽΪ��SiCl4+3H2O=4HCl��+H2SiO3����
�ʴ�Ϊ��SiCl4+3H2O=4HCl��+H2SiO3����
���ڷ�ӦIV�����Ȼ����백����Ӧ����Si��NH2��4��һ�����壬��Ԫ���غ��֪��������ΪHCl���ڷ�ӦV��Si��NH2��4���ȷֽ�����Si3N4����ԭ���غ��֪��һ�ֲ���ΪNH3��
�ʴ�Ϊ��HCl��NH3��
���� ��������ƴ������Ŀ���漰��ѧ�������̡������ƶϡ����ԭ�����Ȼ�ѧ����ʽ��д�ȣ�������ѧ�������Ŀ��飬��Ҫѧ���߱���ʵ�Ļ������������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڶ�����Ԫ���⻯���ȶ���˳����HF��H2O��NH3�����������Ԫ���⻯���ȶ���˳��Ҳ��HCl��H2S��PH3 | |
| B�� | SiO2�����ۻ�ʱ�ƻ����ǹ��ۼ�������CO2�����ۻ�ʱ�ƻ���Ҳ�ǹ��ۼ� | |
| C�� | �ɵ������MgCl2����ȡ����þ��Ҳ�ܵ������AlCl3����ȡ������ | |
| D�� | �������������ӣ����������ӣ��������������ӣ�Ҳ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | F2��F- | B�� | HNO3��NO | C�� | Mg��Mg2+ | D�� | Na2O2��O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | XeO4 | B�� | BeCl2 | C�� | CH4 | D�� | PCl3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ���ݻ�һ�����ܱ������У����淴Ӧ��A2 ��g��+B2��g��?xC��g�� ��������ͼ����ʾ��ϵ���ɴ��ƶϣ���ͼ���˵����ȷ���ǣ�������
���ݻ�һ�����ܱ������У����淴Ӧ��A2 ��g��+B2��g��?xC��g�� ��������ͼ����ʾ��ϵ���ɴ��ƶϣ���ͼ���˵����ȷ���ǣ�������| A�� | P3��P4��Y���ʾ��������ƽ��Ħ������ | |
| B�� | P3��P4��Y���ʾ���������ܶ� | |
| C�� | P3��P4��Y���ʾA2��Ũ�� | |
| D�� | P3��P4��Y���ʾA2��ת���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Ԫ�ر�� | A | B | C | D | E | F | G | H | I | J |
| ԭ�Ӱ뾶��10-10m�� | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| ������� | +6 | +1 | �� | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| ����� | -2 | �� | -2 | �� | -4 | -3 | -1 | �� | -3 | -4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SiO2��SiF4 | B�� | Al2O3��Al��OH��3 | C�� | Fe��FeCl2 | D�� | SiO2��CaSiO3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com