
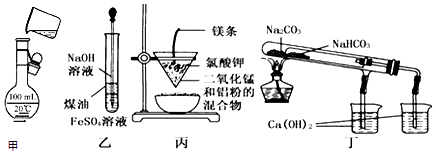
| A. | 用甲图所示装置将溶液定容到100 mL | |
| B. | 用乙图装置制备Fe(OH)2 | |
| C. | 用丙图装置可制得金属锰 | |
| D. | 用丁图装置验证NaHCO3和Na2CO3的热稳定性 |
分析 A.转移液体需要玻璃棒引流,定容需要胶头滴管;
B.煤油可隔绝空气,防止生成的氢氧化亚铁被氧化;
C.点燃Mg条,引发铝热反应,生成Mn;
D.小试管中碳酸氢钠受热温度低,分解生成使石灰水变浑浊的气体.
解答 解:A.转移液体需要玻璃棒引流,定容需要胶头滴管,图中定容操作不合理,故A错误;
B.煤油可隔绝空气,防止生成的氢氧化亚铁被氧化,则图中装置可制备Fe(OH)2,故B正确;
C.点燃Mg条,引发铝热反应,Al与二氧化锰反应生成Mn,故C正确;
D.小试管中碳酸氢钠受热温度低,分解生成使石灰水变浑浊的气体,具有对比性,可验证NaHCO3和Na2CO3的热稳定性,故D正确;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握溶液配制、物质的制备、性质实验、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 846.3 kJ•mol-l | B. | 758.3 kJ•mol-l | C. | 890.3 kJ•mol-l | D. | 714.3 kJ•mol-l |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol NaOH含有0.2NA个NaOH分子 | |
| B. | 3.2 g O2和O3的混合气体中氧原子数为0.25NA | |
| C. | 常温下,1 mol Cl2与过量NaOH溶液反应,转移电子总数为NA | |
| D. | 过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+、Na+、NO3-、CO32- | B. | Mg2+、Cl-、Na+、SO42- | ||
| C. | K+、Cl-、HCO3-、NO3- | D. | Ca2+、Na+、Fe3+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 实验内容 | 实验目的 |
| A | 测定相同物质的量浓度的KOH和氨水的pH | 证明氨水中存在电离平衡 |
| B | 向混有NaCl的NaOH溶液中滴入已知浓度的盐酸(用酚酞作指示剂) | 滴定其中NaOH含量 |
| C | 将Mg、Al和NaOH溶液设计为原电池 | 比较Mg、Al活泼性强弱 |
| D | 用惰性电极电解饱和食盐水,阴极附近滴加酚酞 | 验证阴极有碱生成 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H4=△H3+△H2+△H1 | B. | △H4=△H3+2△H2+2△H1 | ||
| C. | △H4=△H3+2△H2-2△H1 | D. | △H4=△H3+2△H2-△H1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 医疗上常用75%的酒精进行消毒 | B. | 光导纤维的主要成份是二氧化硅 | ||
| C. | 食品行业用小苏打制作发酵粉 | D. | SO2可以随意排放,对环境没有污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
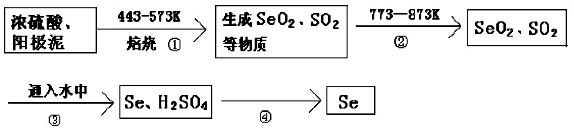
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com