

 ��
�� ��
�� ��
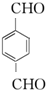
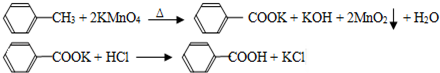
������ A�������ڹ��������£�A����������ȡ����Ӧ����A�ṹ��ʽΪ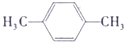 ��B�ܷ���������Ӧ����C��C�ܺ�����������ͭ����Һ����������Ӧ������B�ķ�Ӧ���ȴ�����ˮ�ⷴӦ����B�ṹ��ʽΪ
��B�ܷ���������Ӧ����C��C�ܺ�����������ͭ����Һ����������Ӧ������B�ķ�Ӧ���ȴ�����ˮ�ⷴӦ����B�ṹ��ʽΪ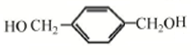 ��CΪ
��CΪ ��DΪ
��DΪ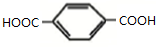 ��D�ͱ���һԪ������������Ӧ����E��E����Ԫ�ص���������Ϊ23%����μӷ�Ӧ�ı���һԪ������ʽΪCnH2n+1OH����E�ķ���ʽΪCn+8H4n+6O4��OԪ����������=$\frac{16��4}{12����8+n��+1����4n+6��+16��4}$��100%=23%��n=4������EΪ�Ա������ᶡ�����ݴ˷������
��D�ͱ���һԪ������������Ӧ����E��E����Ԫ�ص���������Ϊ23%����μӷ�Ӧ�ı���һԪ������ʽΪCnH2n+1OH����E�ķ���ʽΪCn+8H4n+6O4��OԪ����������=$\frac{16��4}{12����8+n��+1����4n+6��+16��4}$��100%=23%��n=4������EΪ�Ա������ᶡ�����ݴ˷������
��� �⣺A�������ڹ��������£�A����������ȡ����Ӧ����A�ṹ��ʽΪ ��B�ܷ���������Ӧ����C��C�ܺ�����������ͭ����Һ����������Ӧ������B�ķ�Ӧ���ȴ�����ˮ�ⷴӦ����B�ṹ��ʽΪ
��B�ܷ���������Ӧ����C��C�ܺ�����������ͭ����Һ����������Ӧ������B�ķ�Ӧ���ȴ�����ˮ�ⷴӦ����B�ṹ��ʽΪ ��CΪ
��CΪ ��DΪ
��DΪ ��D�ͱ���һԪ������������Ӧ����E��E����Ԫ�ص���������Ϊ23%����μӷ�Ӧ�ı���һԪ������ʽΪCnH2n+1OH����E�ķ���ʽΪCn+8H4n+6O4��OԪ����������=$\frac{16��4}{12����8+n��+1����4n+6��+16��4}$��100%=23%��n=4������EΪ�Ա������ᶡ����
��D�ͱ���һԪ������������Ӧ����E��E����Ԫ�ص���������Ϊ23%����μӷ�Ӧ�ı���һԪ������ʽΪCnH2n+1OH����E�ķ���ʽΪCn+8H4n+6O4��OԪ����������=$\frac{16��4}{12����8+n��+1����4n+6��+16��4}$��100%=23%��n=4������EΪ�Ա������ᶡ����
��1��A�ṹ��ʽΪ ��Ϊ�Զ��ױ���DΪ�Ա������ᣬ��D�й�����Ϊ�Ȼ���D����EΪ������Ӧ��ȡ����Ӧ���ʴ�Ϊ���Զ��ױ����Ȼ���ȡ��������������Ӧ��
��Ϊ�Զ��ױ���DΪ�Ա������ᣬ��D�й�����Ϊ�Ȼ���D����EΪ������Ӧ��ȡ����Ӧ���ʴ�Ϊ���Զ��ױ����Ȼ���ȡ��������������Ӧ��
��2���ȴ�������ˮ�ⷴӦ���ɶԶ����״�����Ӧ����ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��3��ͨ�����Ϸ���֪��C�ṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��4��DΪ ��D��ͬ���칹���������������
��D��ͬ���칹���������������
����FeCl2��Һ����ɫ��˵�����з��ǻ���
���ܷ���ˮ�ⷴӦ˵������������
���ܷ���������Ӧ��˵������ȩ����
�ܱ�������3�ֲ�ͬ��������ԭ�ӣ�
���-OH��-OOCH������λ��-CHO��4�ַ��÷�����
���-OH��-OOCH���ڼ�λ��-CHO��4�ַ��÷�����
���-OH��-OOCH���ڶ�λ��-CHO��2�ַ��÷�����
���Է�����������10�֣�
���������ֽṹ��ʽΪ ��
��
�ʴ�Ϊ��10�� ��
��
��5��E�ķ���ʽCl6H22O4������һԪ��Ϊ����������Է���������74�������������ʱ�Ϊ74��
�ʴ�Ϊ��Cl6H22O4��74��
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶ�����������ijЩ���ʽṹ��ʽ����Ӧ������������Ϣ���������ϵķ��������ƶϣ��ѵ���ͬ���칹�������жϣ��������ճ����л�������ż������ʣ���Ŀ�Ѷ��еȣ�


 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д� ��˼άС�ھ�100����ҵ��ϵ�д�
��˼άС�ھ�100����ҵ��ϵ�д� ��ʦָ��һ��ͨϵ�д�
��ʦָ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
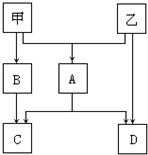 �ס��������ֳ���������Ԫ�صĵ��ʣ����йػ������������ͼ��ʾ������CΪ��ɫ������DΪ���壮
�ס��������ֳ���������Ԫ�صĵ��ʣ����йػ������������ͼ��ʾ������CΪ��ɫ������DΪ���壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
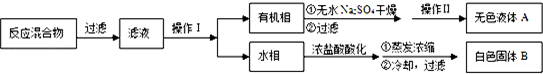
| ��� | ʵ�鷽�� | ʵ������ | ���� |
| �� | ����ɫ����B����ˮ�У������� �⣬��ȴ������ | �õ���ɫ�������ɫ��Һ | ----------------- |
| �� | ȡ������Һ���Թ��У����������������ữ��AgNO3��Һ | ���ɰ�ɫ���� | ��Һ��Cl- |
| �� | �����ɫ���壬����ʹ���ڻ��������۵� | �۵�Ϊ122.4�� | ��ɫ�����DZ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
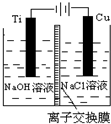 ����Cu2O���ھ��������Ĵ����ܶ��ܵ���ע���������ӽ���Ĥ�����������Һ��OH-��Ũ���Ʊ�����Cu2O��װ����ͼ��ʾ���ܷ�ӦΪ2Cu+H2O$\frac{\underline{\;���\;}}{\;}$Cu2O+H2��������˵������ȷ���ǣ�������
����Cu2O���ھ��������Ĵ����ܶ��ܵ���ע���������ӽ���Ĥ�����������Һ��OH-��Ũ���Ʊ�����Cu2O��װ����ͼ��ʾ���ܷ�ӦΪ2Cu+H2O$\frac{\underline{\;���\;}}{\;}$Cu2O+H2��������˵������ȷ���ǣ�������| A�� | �ѣ�Ti���缫���淢��������Ӧ | |
| B�� | ����������Һ��pH��С | |
| C�� | ���ӽ���Ĥ�˲��������ӽ���Ĥ | |
| D�� | ���������ܷ�Ӧʽ�ǣ�2Cu+2OH--2e-�TCu2O+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
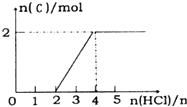 A��B��C��D��E �ֱ������ѧ��ѧ�еij������ʣ��������ĿҪ��ش��������⣺
A��B��C��D��E �ֱ������ѧ��ѧ�еij������ʣ��������ĿҪ��ش��������⣺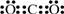 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
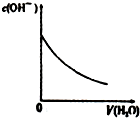 | 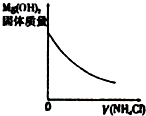 | 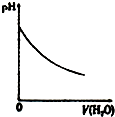 | 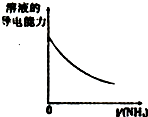 |
| A�������ˮϡ�� | B��Mg��OH��2����Һ�еμ�NH4Cl��Һ | C��NH4Clϡ��Һ��ˮϡ�� | D��NH3ͨ�������Һ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼����������ϣ�2H++CO32-�TCO2��+H2O | |
| B�� | AlͶ��NaOH��Һ�У�Al+OH-+H2O�TAlO2-+H2�� | |
| C�� | ����������Һ��ϡ�����ϣ�2H++SO32-�TSO2��+H2O | |
| D�� | ����������Ũ�����Ϻ���ȣ�MnO2+4H++4Cl-�TMnCl2+Cl2��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
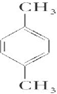 ��
��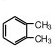 ��
�� ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com