
【题目】研究氮及其化合物对化工生产有重要意义。
(1)已知:N2(g)+O2(g)=2NO(g); △H=+180 kJ·mol-1
4NH3(g)+5O2(g) =4NO(g)+6H2O(g); △H= -908 kJ·mol-1
请写出氨气被一氧化氮氧化生成无毒气体的热化学方程式:___________。
(2)工业合成氨的原理为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1。下图甲表示在一定体积的密闭容器中反应时N2的物质的量浓度随时间的变化,图乙表示在其他条件不变的情况下,改变起始投料中H2与N2的物质的量之比(设为k)对该平衡的影响。
2NH3(g) ΔH=-92.4 kJ·mol-1。下图甲表示在一定体积的密闭容器中反应时N2的物质的量浓度随时间的变化,图乙表示在其他条件不变的情况下,改变起始投料中H2与N2的物质的量之比(设为k)对该平衡的影响。

①已知图甲中0~t1 min内,v(H2)=0.03 mol·L-1·min-1,则t1=________ min;若从t2 min起仅改变一个反应条件,则所改变的条件可能是____________________________(填一种即可)。
②图乙中,b点时k=_________。
③已知某温度下该反应的平衡常数K=10,在该温度下向容器中同时加入下列浓度的混合气体:c(H2)=0.1 mol/L,c(N2)=0.5 mol/L,c(NH3)=0.1 mol/L,则在平衡建立过程中NH3的浓度变化趋势是__________(填“逐渐增大”“逐渐减小”或“恒定不变”)。
(3)联氨(又称肼,N2H4,无色液体)为二元弱碱,在水中的电离方式与氨相似,是一种应用广泛的化工原料,可用作火箭燃料。(已知:N2H4+H+![]() N2H5+)
N2H5+)
①N2H5+的电子式为_______。联氨与硫酸形成的酸式盐的化学式为________。
②联氨是一种常用的还原剂。向装有少量AgCl的试管中加入联氨溶液,观察到的现象___________________________________________________________。
(4)尿素(CO(NH2)2)是目前使用量较大的一种化学氮肥,工业上利用下图所示装置(阴、阳极均为惰性电极)电解尿素的碱性溶液制取氢气。
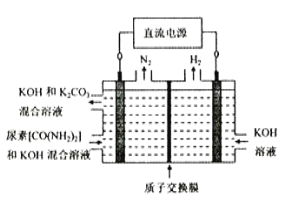
①该装置中阳极的总电极反应式为_____________________________________________。
②若两极共收集到气体22.4L(标准状况),则消耗的尿素为____________g(忽略气体的溶解)。
【答案】4NH3(g) + 6NO(g)=5N2(g) + 6H2O(g) ΔH=-1808 kJ·mol-1 30 降低温度(或增大H2浓度、减小NH3浓度) 3:1 逐渐减小 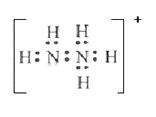 N2H6(HSO4)2 固体逐渐变黑,并有气泡产生 CO(NH2)2+8OH--6e-===N2↑+CO32—+6H2O 15
N2H6(HSO4)2 固体逐渐变黑,并有气泡产生 CO(NH2)2+8OH--6e-===N2↑+CO32—+6H2O 15
【解析】
(1)由盖斯定律计算可得;
(2)①由速率之比等于化学计量数之比,然后根据速率的计算公式求出时间。根据影响化学平衡的因素来解答;
②当N2与H2的起始体积比符合方程式中化学计量数之比时,达到平衡时氨的体积分数最大;
③根据浓度商和化学平衡常数比较,判断化学平衡移动方向,进而判断平衡建立过程中NH3的浓度变化趋势;
(3)①N2H4是二元弱碱,其性质与氨气相似,第一步电离出1个氢氧根离子和N2H5+,则第二步中N2H5+电离出1个氢氧根离子和N2H62+;
(1)令①:N2(g)+O2(g)=2NO(g) △H=+180 kJ·mol-1,②:4NH3(g)+5O2(g) =4NO(g)+6H2O(g) △H= -908 kJ·mol-1,氨气被一氧化氮氧化生成无毒气体的化学方程式为③:4NH3(g) + 6NO(g)=5N2(g) + 6H2O(g),③=②-5![]() ①,△H=(-908-5
①,△H=(-908-5![]() 180)kJ·mol-1=-1808 kJ·mol-1,则氨气被一氧化氮氧化生成无毒气体的热化学方程式4NH3(g) + 6NO(g)=5N2(g) + 6H2O(g) ΔH=-1808 kJ·mol-1;
180)kJ·mol-1=-1808 kJ·mol-1,则氨气被一氧化氮氧化生成无毒气体的热化学方程式4NH3(g) + 6NO(g)=5N2(g) + 6H2O(g) ΔH=-1808 kJ·mol-1;
(2)①0~t1 min内,v(H2)=0.03 mol·L-1·min-1,,v(N2)=0.01 mol·L-1·min-1,则![]() =
=![]() =0.01 mol·L-1·min-1,解得t1=30min。从t2 min起N2的浓度逐渐减小,则所改变的条件可能是降低温度(或增大H2浓度、减小NH3浓度)使得平衡正向移动引起的;
=0.01 mol·L-1·min-1,解得t1=30min。从t2 min起N2的浓度逐渐减小,则所改变的条件可能是降低温度(或增大H2浓度、减小NH3浓度)使得平衡正向移动引起的;
②当N2与H2的起始体积比符合方程式中化学计量数之比时,达到平衡时氨的体积分数最大,即图乙中,b点时k=3:1;
③c(H2)=0.1 mol/L,c(N2)=0.5 mol/L,c(NH3)=0.1 mol/L,则Qc= =
=![]() =20>10,所以反应逆向进行,NH3的浓度逐渐减小;
=20>10,所以反应逆向进行,NH3的浓度逐渐减小;
(3)①N2H4是二元弱碱,其性质与氨气相似,第一步电离出1个氢氧根离子和N2H5+,则第二步中N2H5+电离出1个氢氧根离子和N2H62+。N2H5+的电子式为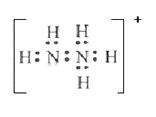 。N2H4是二元弱碱,其性质与氨气相似,第一步电离出1个氢氧根离子和N2H5+,则第二步中N2H5+电离出1个氢氧根离子和N2H62+,则联氨与硫酸形成的酸式盐的化学式为N2H6(HSO4)2;
。N2H4是二元弱碱,其性质与氨气相似,第一步电离出1个氢氧根离子和N2H5+,则第二步中N2H5+电离出1个氢氧根离子和N2H62+,则联氨与硫酸形成的酸式盐的化学式为N2H6(HSO4)2;
②Nspan>2H4被银离子氧化,银离子被还原生成单质银,-2价的N元素被氧化为N2,反应方程式为:N2H4+4AgBr=4Ag↓+N2↑+4HBr,因此反应出现现象为:固体逐渐变黑,并有气泡产生;
(4)①阳极化合价升高失去电子,发生氧化反应,CO(NH2)2被氧化为N2,在碱性条件下产生碳酸根离子,则该装置中阳极的总电极反应式为CO(NH2)2+8OH--6e-=N2↑+CO32—+6H2O;
②该电解池总反应式为:CO(NH2)2+2OH-=N2↑+CO32—+3H2↑,若两极共收集到气体22.4L(标准状况),即1mol气体,其中氮气和氢气的物质的量之比为1:3,故氮气有0.25mol,CO(NH2)2的物质的量也为0.25mol,则消耗的尿素为0.25mol ![]() 15g。
15g。


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案科目:高中化学 来源: 题型:
【题目】钛的电解冶炼法,如图所示。以含少量CaC12的CaO熔融物作为介质,电解时阴极生成的Ca进一步还原TiO2得到钛。下列说法不正确的是
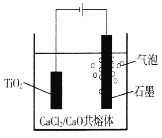
A. Ca还原TiO2的化学方程式为2Ca+TiO2===Ti+2CaO
B. 阳极石墨稳定性强,在实际生产过程中质量几乎不会改变
C. CaC12的作用可能是增强导电性,同时起到助熔剂的作用
D. 已知F=96500C·mol-1,当I=0.5A,通电80分钟,理论上可得Ti的质量为(0.5×80×60×48)/4×96500g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下为中学化学中常见的物质:①Cu; ②FeCl3溶液; ③CuCl2溶液;④CO2;⑤H2SO4;⑥酒精;⑦CaCO3;⑧FeSO4;⑨Ba(OH)2。
请根据要求回答下列有关问题:
(1)以上物质中属于电解质的是________;属于非电解质的是__________。(填序号)
(2)将②③⑧混合配制成浓度均为1molL﹣1的混合溶液100mL,加入一定量的铁粉,充分反应后,若铁粉无剩余,且有铜生成.则反应后的溶液中一定含有的阳离子是______,发生反应的离子方程式为_____________________________________________________。
(3)检验②溶液中阳离子的试剂是________________,证明其存在的现象是____________。
(4)向沸水中逐滴滴加1 mol·L-1 FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是________ nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲、乙两个装置的烧杯中分别盛有足量的CuCl2溶液。
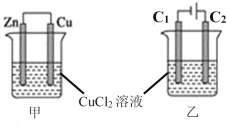
(1)甲装置中,Zn电极发生______反应(填“氧化”或“还原”),溶液中Cl-向_____极(填“Zn”或“Cu”)移动,Zn电极反应式为_______,若反应过程中有0.1mol电子发生转移,则Cu极质量增加__________。
(2)乙装置中,石墨电极C1是_______极,现象是______,C2极电极反应式为_______,若反应过程中阴极析出12.8g的Cu,则阳极产生的气体在标准状况下的体积为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL K2CO3与KAlO2的混合溶液中逐滴加入1mol·L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+离子的物质的量与加入盐酸溶液的体积变化关系,如图所示。下列说法正确的是

A. a点溶液中:c(HCO3-)+c(H2CO3)+c(H+)=c(OH-)
B. b点所得溶液中阴离子浓度大小顺序为:c(Cl-)>c(HCO3-)>c(CO32-)>c(OH-)
C. c点溶液中:c(Cl-)+c(HCO3-)+c(H2CO3)+c(CO32-)=1.5 mol·L-1
D. d→e的过程中水的电离程度逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和c(H+)都相等,向两烧杯中同时加入两颗锌粒,反应结束后得到等量的氢气,有一个烧杯中有锌粒剩余。下列说法正确的是
A. 两烧杯中参加反应的锌等量
B. 盐酸物质的量浓度比醋酸大
C. 乙烧杯中的锌粒剩余
D. 甲烧杯的反应时间更短
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应速率和限度与生产、生活密切相关。
(1)某同学为了探究锌与硫酸反应过程中的速率变化,在 400mL 稀硫酸中加入足量的锌粉,标况下用排水集气法收集反应放出的氢气,实验记录如下(累计值):
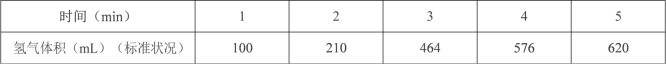
①哪一时间段反应速率最大_______min(填“0~1”、“1~2”、“2~3”、“3~4”、“4~5”), 原因是________。
②求 3~4 分钟时间段以盐酸的浓度变化来表示的该反应速率________设溶液体积不变)。
(2)该同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回 答下列问题:
①硫酸铜溶液可以加快氢气生成速率的原因是_______。
②实验室中现有 Na2SO4、MgSO4、Ag2SO4、K2SO4 等 4 种溶液,可与实验中 CuSO4 溶液起相似作用的是_______。
③要减慢上述实验中气体产生速率,可采取的合力措施有_______、_______(答两种)。
(3) 某温度下在 4 L 密闭容器中,X、Y、Z 三种气态物质的物质的量随时间变化曲线如图。
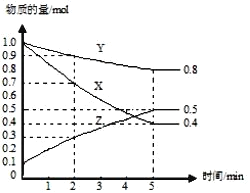
①该反应的化学方程式是_______。
②该反应达到平衡状态的标志是_______(填字母)
A.Y 的体积分数在混合气体中保持不变 B.X、Y 的反应速率比为 3:1
C.容器内气体压强保持不变 D.容器内气体的总质量保持不变E.生成 1 mol Y 的同时消耗 2 mol Z
③2 min 内 Y 的转化率为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种镁-过氧化氢燃料电池的原理为Mg + H2O2 + H2SO4=MgSO4+ 2H2O ,其装置如图所示。下列说法错误的是

A.a极发生还原反应B.电子由b极经电解质溶液流向a极
C.Mg2+由右侧经过阳离子交换膜移向左侧D.b极电极反应式为Mg-2e-=Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学在实验室以下图所示的仪器和药品,进行氯气和铜粉反应的实验(部分夹持装置已省略).请按要求回答下列问题:

(1)装置A烧瓶中发生反应的化学方程式为________________________。
(2)按气流方向连接各仪器接口的顺序是(填接口字母):
a→_____、_____→_____、_____→f→g→_____
(3)装置C中饱和食盐水的作用是__________________________。
(4)装置B中发生反应的离子方程式为_____________________________。
(5)加热装置D时,铜粉发生反应的化学方程式为___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com