
| 实验序号 | 实验现象 | 实验结论 |
| A | 氯水呈浅黄绿色 | 氯水中含有Cl2 |
| B | 向FeCl2溶液中滴加氯水,溶液变成棕黄色 | 氯水中含有HClO |
| C | 向氯水中滴加硝酸酸化的 AgNO3溶液,产生白色沉淀 | 氯水中含有Cl- |
| D | 向氯水中加入NaHCO3粉末,有气泡产生 | 氯水中含有H+ |
| A. | A | B. | B | C. | C | D. | D |
分析 氯气溶液水得到的溶液为氯水,氯水中,氯气大部分以分子形式存在,少量氯气与水反应生成氯化氢和次氯酸,氯化氢为强电解质完全电离生成氢离子和氯离子,次氯酸为弱电解质部分电离,生成氢离子和次氯酸根离子,据此解答.
解答 解:A.氯气为黄绿色气体,氯水呈浅绿色,是因为溶解了氯气,故A正确;
B.向FeCl2溶液中滴加氯水,溶液变成棕黄色,是因为发生反应2FeCl2+Cl2=2FeCl3,故B错误;
C.氯气与水反应生成氯化氢和次氯酸,氯化氢为强电解质完全电离生成氢离子和氯离子,氯离子与银离子反应生成氯化银沉淀,故C正确;
D.向氯水中加入NaHCO3粉末,有气泡产生,是因为,碳酸氢根离子与氯水中的氢离子发生反应生成水和二氧化碳,故D正确;
故选:B.
点评 本题考查了氯水的性质,侧重考查学生对基础知识的掌握,为高考的频考点,明确氯水的成分是解题关键,注意对基础知识的积累.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
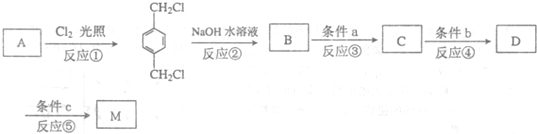
 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$ +2NaCl
+2NaCl 有多种同分异构体,其中含有苯环且苯环上只有两个取代基的同分异构体的数目为11(不含本身),其中核磁共振氢谱有3种峰的结构简式为
有多种同分异构体,其中含有苯环且苯环上只有两个取代基的同分异构体的数目为11(不含本身),其中核磁共振氢谱有3种峰的结构简式为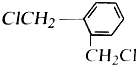
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


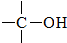 +
+ $→_{△}^{H_{2}SO_{4}(浓)}$
$→_{△}^{H_{2}SO_{4}(浓)}$ +H2O
+H2O +R′CHO$\stackrel{一定条件}{→}$
+R′CHO$\stackrel{一定条件}{→}$
 .
. .
. .
.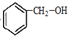 ,名称是苯甲醇.
,名称是苯甲醇. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
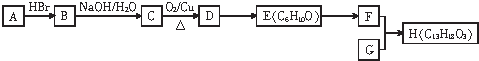
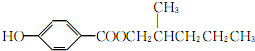
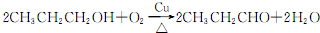
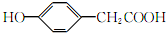 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com