
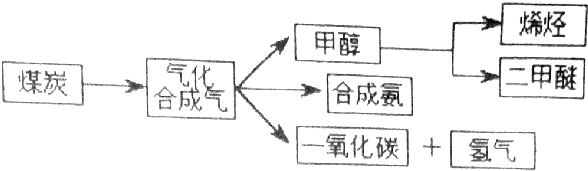
分析 I.根据平衡常数表达式可写成化学方程式;
Ⅱ.(1)运用盖斯定律按照目标方程式将已知的热化学方程式变形运算得到所要求得目标反应的热化学方程式;反应③为放热反应降低温度平衡正向移动K值增大;
(2)列三段表示出反应达到平衡过程中各物质的浓度,运用反应速率表达式求出5min内CO的平均反应速率,应用K求出a值.
解答 解:Ⅰ.因为K=$\frac{C({H}_{2})•C(CO)}{C({H}_{2}O)}$,所以该反应的方程式为:C(s)+H2O(g)?CO(g)+H2(g),注意C为固态,不列入平衡常数表达式,
故答案为:C(s)+H2O(g)?CO(g)+H2(g);
Ⅱ.(1)①CO(g)+2H2(g)?CH3OH(g)△H1=-90.7kJ•mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-23.5kJ•mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-41.2kJ•mol-1
依据盖斯定律将方程式变形①×2+②+③得 3CO(g)+3H2(g)=CH3OCH3(g)+CO2(g),△H=△H1×2+△H2+△H3=-246.1kJ•mol-1
反应③为放热反应降低温度平衡正向移动K值增大,830℃时反应③的K=1.0,催化反应室中温度为230~280℃,所以K值增大,K>1.0;
故答案为:3CO(g)+3H2(g)=CH3OCH3(g)+CO2(g)△H=-246.1kJ•mol-1;>;
(2)CO(g)+2H2(g)?CH3OH(g)
起始浓度( mol/L) 1 2.4 0
转化浓度( mol/L) 0.5 1 0.5
平衡浓度( mol/L) 0.5 1.4 0.5
△C(CO)=1×0.5=0.5
V(CO)=△C(CO)÷t=0.5mol/L÷5min=0.1mol/(L•min);
K=$\frac{[CH{\;}_{3}OH]}{[CO][H{\;}_{2}]{\;}^{2}}$=$\frac{0.5}{0.5×1.4{\;}^{2}}$=$\frac{1}{1.4{\;}^{2}}$
CO(g)+2H2(g)?CH3OH(g)
起始浓度( mol/L) 4 a 0
转化浓度( mol/L) 2 4 2
平衡浓度( mol/L) 2 a-4 2
因为温度相同所以改变初始浓度后平衡常数不变K=$\frac{2}{2×(a-4){\;}^{2}}$=$\frac{1}{1.4{\;}^{2}}$
a=5.4mol/L;
故答案为:0.1mol/(L•min); 5.4.
点评 本题考查了盖斯定律求反应热、化学平衡常数表达式及其应用,难度中等,注意平衡常数的应用.


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:选择题
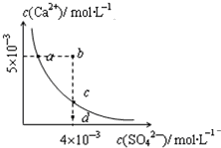 常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水溶液中的沉淀溶解平衡曲线见如图.下列说法不正确的是( )
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水溶液中的沉淀溶解平衡曲线见如图.下列说法不正确的是( )| A. | CaSO4溶解在水中,c(Ca2+)=c(SO42-)=3×10-3mol/L | |
| B. | 在d点溶液中加入一定量的CaCl2可能会有沉淀析出 | |
| C. | a点对应的Ksp等于c点对应的Ksp | |
| D. | b点将有沉淀生成,平衡后溶液中c(SO42-)等于3×10-3mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到化学平衡时,正反应速率与逆反应速率不相等 | |
| B. | 反应过程中,Y的单质的体积分数始终为50% | |
| C. | 达到化学平衡时,X、Y的两种单质在混合气体中的物质的量之比为1:1 | |
| D. | 达到化学平衡的过程中,混合气体平均相对分子质量逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 碳及其化合物在人类生产、生活中的应用非常广泛.“低碳生活”不再只是一种理想,更是一种值得期待的生活方式.
碳及其化合物在人类生产、生活中的应用非常广泛.“低碳生活”不再只是一种理想,更是一种值得期待的生活方式.| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | CO2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | D | t |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度( oC) | 15.0 | 25.0 | 30.0 | 35.0 |
| K/(×10-8 mol3•L-3) | 0.205 | 1.64 | 4.68 | 10.8 |
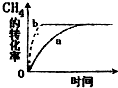
| A. | 若Z的体积分数不再随时间变化时表示反应达平衡状态 | |
| B. | 35 oC时,达平衡时,X分解了 0.03 mol | |
| C. | 该反应在高温下可能自发 | |
| D. | 若在恒温下,压缩容器体积,再次达平衡后,n(X)比原平衡大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯与苯都能使溴水褪色,但褪色原理不同 | |
| B. | 1 mol乙烯与Cl2完全加成,然后与Cl2发生取代反应,共消耗氯气5mol | |
| C. | 溴水遇到乙醛溶液出现褪色现象,是因为它们发生了氧化反应 | |
| D. | 二氯甲烷存在两种不同的结构 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com