
| A. | 煤油 | B. | 液态煤 | C. | 煤焦油 | D. | 甲醇 |
科目:高中化学 来源: 题型:解答题
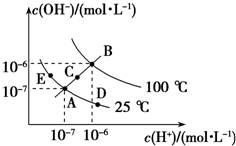 已知水的电离平衡曲线如图所示,试回答下列问题:
已知水的电离平衡曲线如图所示,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火时,用细沙覆盖灭火 | |
| B. | 金属钠与氧气反应,条件不同,产物不同 | |
| C. | Na的化学性质比镁活泼,故用Na与MgCl2溶液反应制取金属镁 | |
| D. | 9.2g金属钠与足量水反应,反应过程中有0.4mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
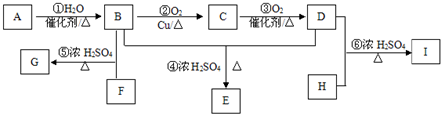
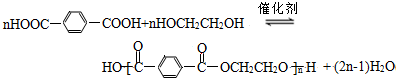 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
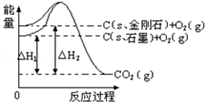
| A. | 金刚石的稳定性强于石墨 | |
| B. | 12g石墨总键能比12g金刚石小1.9kJ | |
| C. | 石墨和金刚石的转化是物理变化 | |
| D. | C(s、石墨)=C(s、金刚石)△H=+1.9 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1CaCl2溶液中含氯离子数为0.2 NA | |
| B. | 0.1 mol铁粉与过量的氯气完全反应,转移电子数为0.2NA | |
| C. | 标准状况下,2.24 L H2O所含的原子总数为0.3 NA | |
| D. | 常温常压下,17g NH3含有的电子个数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaClO是“84消毒液”的有效成分,其水溶液能使有色布条褪色,反应中NaClO表现还原性 | |
| B. | Cl2与烧碱溶液反应的实质是Cl2+OH-═Cl-+ClO-+H2O | |
| C. | 氯气有毒,在通风橱中制备氯气可以消除氯气的污染 | |
| D. | 将Cl2通入淀粉-KI溶液,溶液变蓝色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com