
常温常压下,可能含有N2、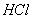 、CO、CO2的混合气体,依次通过足量的碳酸氢钠溶液和灼热的氧化铜,恢复到原来的温度和压强,气体体积没有变化;再通过足量的氧化钠,气 体积减少,最后通过灼热的铜网,恢复到原来的温度压强,体积又减少,并有剩余气体,若上述各步反应均完全,则对混合成分的判断正确的是( )
、CO、CO2的混合气体,依次通过足量的碳酸氢钠溶液和灼热的氧化铜,恢复到原来的温度和压强,气体体积没有变化;再通过足量的氧化钠,气 体积减少,最后通过灼热的铜网,恢复到原来的温度压强,体积又减少,并有剩余气体,若上述各步反应均完全,则对混合成分的判断正确的是( )
A、一定有N2和CO2,可能有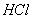 和CO
和CO
B、一定有N2,且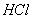 、CO、CO2中至少含有一种
、CO、CO2中至少含有一种
C、一定有N2、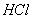 、CO、CO2
、CO、CO2
D、一定有N2、CO、CO2,一定没有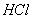
科目:高中化学 来源: 题型:
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢或锂电池的十倍,可连续使用一个月才充一次电,其电池反应为: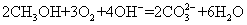 ,则下列有关说法不正确的是
,则下列有关说法不正确的是
A、放电时化学能转变为电能 B、放电时 参与正极反应
参与正极反应
C、充电时阴极产生 D、充电时每生成1mol
D、充电时每生成1mol ,则转移6mol电子
,则转移6mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
对于在密闭容器中进行的反应:N2+O2 2NO,下列不能加快该反应的反应速率的条件是
2NO,下列不能加快该反应的反应速率的条件是
A.体积增大到原的2倍 B.充入更多的NO C.缩小体积 D.升高温度

查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y是原子核电荷数不大于18的元素。若X、Y两元素化合物组成是YX3,已知X原子的最外层电子数为a+2,次外层电子数为a+3;Y原子的最外层电子数为b-3,次外层电子数为b。则a和b的值分别是( )
A、3,2 B、2,3 C、5,6 D、5,8
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组利用以下材料来探究NH3的还原性,部分实验装置如图所示。
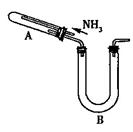
|
材料二:Cu+在酸性溶液中不稳定,可发生自身氧化还原反应生成Cu2+和Cu,Cu2O+2H+=Cu2++Cu+H2O。
请回答下列问题:
(1)在实验室里,该学习小组设计下列制取纯净干燥氨气的方案,简易、可行的最佳方案是 。
A、加热氯化铵固体,再通过碱石灰。
B、在N2和H2的混合气体中加入铁触媒,并加热至500℃,再通过碱石灰。
C、加热浓氨水,再通过碱石灰。
D、在生石灰中加入浓氨水,再通过碱石灰。
(2)为证明NH3还原CuO的反应中有水生成,B中应放入的试剂是 。
(3)当观察到 (填现象),即表明A中的反应已经完成。
(4)该小组欲用体积比为1:4的稀硫酸作试剂,检验反应是否有Cu2O固体生成。现用98%的浓硫酸配制1:4的稀硫酸,所需的玻璃仪器除了胶头滴管外还有 。可证明还原产物中含有Cu2O的操作及现象是 。
(5)请写出A中生成Cu2O的化学方程式 。
(6)若用定量的方法测定该反应是否生成Cu2O,最简便且准确的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
以色列科学家达尼埃尔·谢赫特曼因发现“准晶体”独获2011年诺贝尔化学奖。某准晶体W由一定比例的铁、铜、铝组成,取两小块该准晶体:一块投入烧杯①中,注入浓氢氧化钠溶液浸没固体;另一块投入烧杯②中,注入稀硫酸浸没固体。下列分析合理的是
A.烧杯①中,若构成微型电池,负极反应式为2Al-6e-=2Al3+,正极反应式为
6H++6e-=3H2↑
B.烧杯①中,若将电解质溶液换成浓硝酸,构成微型电池时铝为负极,铜为正极,
C.烧杯②中,若铁、铜构成微型电池,则铁为负极;若铝、铁构成微型电池,则铁为正极
D.烧杯②中,固体最终完全溶解,溶液呈蓝色。向溶液中滴加KSCN溶液,溶液不变色。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物的说法中,正确的一组是( )
①淀粉、油脂、蛋白质在一定条件下都能发生水解反应
②淀粉和纤维素互为同分异构体
③食用油属于酯类,石蜡油属于烃类
④石油的分馏和煤的气化都是发生了化学变化
⑤淀粉遇碘酒变蓝色,在加热条件下葡萄糖能与新制的氢氧化铜悬浊液发生反应
A.②③④ B.①②④ C.①③⑤ D.②④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com