
【题目】某烯烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型。根据如图回答下列问题:

(1)写出D的结构简式:__________。
(2)②的反应类型是__________。
(3)写出④的化学反应方程式:________________________________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列关于甲、乙、丙、丁四种有机物说法正确的是( )

A. 甲、乙、丙、丁中加入NaOH的醇溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,均有沉淀生成
B. 甲中加入NaOH的水溶液共热,再滴入AgNO3溶液,可检验该物质中含有的卤素原子
C. 乙发生消去反应得到两种烯烃
D. 丙与NaOH的水溶液共热,反应后生成的醇能被氧化为醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法错误的是
A. 玻璃、水泥、陶瓷都为硅酸盐产品
B. 目前我国流通的硬币都是由合金材料制造的
C. 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用
D. 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生产和日常生活中有着重要的应用,下列叙述正确的是
A. 白酒中混有少量的塑化剂,少量饮用对人体无害,可以通过过滤的方法除去
B. 将猕猴桃和苹果放在一起,猕猴桃更容易成熟。是因为苹果释放的乙烯具有催熟作用
C. 氨气可以做制冷剂,是因为氨气有一定的还原性
D. 大分子化合物油脂在人体内水解为氨基酸和甘油等小分子,才能被人体吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】扁桃酸衍生物是重要的医药中间体,以A和B 为原料合成扁桃酸衍生物F路线如下:

(1)A的分子式为C2H2O3,可发生银镜反应,且具有酸性,A所含官能团名称为:_________。写出A+B→C的化学反应方程式__________________________。
(2)C 中①、②、③3个—OH的酸性由强到弱的顺序是:_______。
中①、②、③3个—OH的酸性由强到弱的顺序是:_______。
(3)E是由2分子C生成的含有3个六元环的化合物,E的分子中不同化学环境的氢原子有_____种。
(4)D→F的反应类型是______,1mol F在一定条件下与足量NaOH溶液反应,最多消耗NaOH的物质的量为_______mol。写出符合下列条件的F的所有同分异构体(不考虑立体异构)的结构简式____。
①属于一元酸类化合物 ②苯环上只有2个取代基且处于对位,其中一个是羟基
(5)已知:![]() 。A有多种合成方法,在方框中写出由乙酸合成A的路线流程图(其他原料任选)合成路线流程图示例如下:
。A有多种合成方法,在方框中写出由乙酸合成A的路线流程图(其他原料任选)合成路线流程图示例如下:

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑦种元素,根据题意回答以下问题:

(1)在③~⑦五种元素中,原子半径最大的是____________(填元素符号);
(2)②的原子结构示意图为__________;
(3)①~⑦对应元素中最高价氧化物对应的水化物酸性最强的是________(填化学式,下同),呈两性的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱土金属指II A族的铍(Be)、镁(Mg)、钙(Ca)、锶(Sr)、钡(Ba)等元素,它们的单质及其化合物有着广泛的用途。
(1)Be基态原子的轨道表示式为_________________________;
镁和铝的笫二电离能:I2(Mg)_____I2(Al) (填“>”“ <”或“=”)。
(2)在500~600℃气相中,氯化铍以二聚体Be2Cl4, ( )的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。
)的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。
①在二聚体Be2Cl4中Be的杂化方式为___________,1mol Be2Cl4中含有_________mol 配位键。
②MgCl2的熔、沸点比BeCl2高的原因是____________________。
(3)根据巴索洛规则:一般来讲,盐中阴、阳离子半径相差较大时,其溶解度较大。则在水中溶解度 S(SrF2)____S(BaF2) (填“>” “<””或“=”)。
(4)石灰氮(CaCN2)—种碱性肥料,可用作除草剂、杀菌剂、杀虫剂等。
①CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和________(填化学式),写出CN22-的电子式___________。
②CaCN2与水反应生成CaCO3和NH3两种物质,则1mol CaCN2与水反应的过程中,反应物断裂的σ键总数_______________。
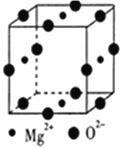
(5) Mg2+与Ni2+、 O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为_________。已知该品胞参数a pm.则该晶体的密度为_________g·cm-3(用a和NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室通常用氧化剂+浓盐酸―→金属氯化物+水+氯气的原理制取少量Cl2。现将一定质量的NaClO放入50 mL 12.00 mol·L-1的浓盐酸中,生成的Cl2在标准状况下的体积为1.12 L。试计算(反应前后溶液的体积变化忽略不计):
(1)反应过程中,被氧化的HCl的物质的量为________ mol。
(2)反应后溶液中HCl的物质的量浓度为______mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 纤维素、光导纤维、淀粉、蛋白质都是由高分子化合物组成的物质
B. 点燃爆竹后,硫燃烧生成SO3
C. 六水合氯化钙可用作食品干燥剂
D. 食用花生油和鸡蛋清都能发生水解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com