
”¾ĢāÄæ”æĻņĢå»żĪŖ2LµÄČŻĘ÷ÖŠ¼ÓČė1mol N2ŗĶ6mol H2½ųŠŠæÉÄę·“Ó¦£ŗN2+3H22NH3 £¬ 2minŗó²āµĆN2µÄĪļÖŹµÄĮæĪŖ0.6mol£¬Ōņ£ŗ
£Ø1£©2minÄŚ£¬N2µÄĪļÖŹµÄĮæ¼õÉŁĮĖ0.4mol£¬H2µÄĪļÖŹµÄĮæ¼õÉŁĮĖmol£¬NH3µÄĪļÖŹĮæŌö¼ÓĮĖmol£®
£Ø2£©ČōÓĆN2µÄÅØ¶Č±ä»ÆĄ“±ķŹ¾øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹ£¬Ōņv£ØN2£©=mol/£ØLmin£©£®
£Ø3£©ČōÓĆH2µÄÅØ¶Č±ä»ÆĄ“±ķŹ¾øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹ£¬Ōņv£ØH2£©=mol/£ØLmin£©£®
£Ø4£©ČōÓĆNH3µÄÅØ¶Č±ä»ÆĄ“±ķŹ¾øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹ£¬Ōņv£ØNH3£©=mol/£ØLmin£©£®
”¾“š°ø”æ
£Ø1£©1.2£»0.8
£Ø2£©0.1
£Ø3£©0.3
£Ø4£©0.2
”¾½āĪö”æ½ā£ŗĻņĢå»żĪŖ2LµÄČŻĘ÷ÖŠ¼ÓČė1mol N2ŗĶ6mol H2½ųŠŠæÉÄę·“Ó¦£ŗN2+3H22NH3 £¬ 2minŗó²āµĆN2µÄĪļÖŹµÄĮæĪŖ0.6mol£¬ŌņĮŠČż¶ĪŹ½£ŗ
N2+ | 3H2 | 2NH3 | ||
ĘšŹ¼Įæ£Ømol£© | 1 | 6 | 0 | |
±ä»ÆĮæ£Ømol£© | 0.4 | 1.2 | 0.8 | |
2minÄ©Įæ£Ømol£© | 0.6 | 4.4 | 0.8 |
”¤£Ø1£©Ōņ2minÄŚ£¬N2µÄĪļÖŹµÄĮæ¼õÉŁĮĖ0.4mol£¬H2µÄĪļÖŹµÄĮæ¼õÉŁĮĖ1.2mol£¬NH3Ōö¼ÓĮĖ0.8mol£»
ĖłŅŌ“š°øŹĒ£ŗ1.2£» 0.8£»£Ø2£©ÓĆN2µÄÅØ¶Č±ä»ÆĄ“±ķŹ¾øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹ£¬Ōņv£ØN2£©= ![]() =
= ![]() =0.1mol/£ØLmin£©£»
=0.1mol/£ØLmin£©£»
ĖłŅŌ“š°øŹĒ£ŗ0.1£»£Ø3£©ÓĆH2µÄÅØ¶Č±ä»ÆĄ“±ķŹ¾øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹ£¬Ōņv£ØH2£©= ![]() =0.3mol/£ØLmin£©£»
=0.3mol/£ØLmin£©£»
ĖłŅŌ“š°øŹĒ£ŗ0.3£»£Ø4£©ÓĆNH3µÄÅØ¶Č±ä»ÆĄ“±ķŹ¾øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹ£¬Ōņv£ØNH3£©= ![]() =0.2mol/£ØLmin£©£»
=0.2mol/£ØLmin£©£»
ĖłŅŌ“š°øŹĒ£ŗ0.2£®
”¾æ¼µć¾«Īö”æ¹ŲÓŚ±¾Ģāæ¼²éµÄ»ÆŃ§Ę½ŗāµÄ¼ĘĖć£¬ŠčŅŖĮĖ½ā·“Ó¦Īļ×Ŗ»ÆĀŹ=×Ŗ»ÆÅØ¶Č”ĀĘšŹ¼ÅØ¶Č”Į100%=×Ŗ»ÆĪļÖŹµÄĮæ”ĀĘšŹ¼ĪļÖŹµÄĮæ”Į100%£»²śĘ·µÄ²śĀŹ=Źµ¼ŹÉś³É²śĪļµÄĪļÖŹµÄĮæ”ĀĄķĀŪÉĻæɵƵ½²śĪļµÄĪļÖŹµÄĮæ”Į100%²ÅÄÜµĆ³öÕżČ·“š°ø£®


 Š”ѧ½Ģ²ÄČ«²āĻµĮŠ“š°ø
Š”ѧ½Ģ²ÄČ«²āĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻĢāŅā½ā“š
£Ø1£©ŌŚ·“Ó¦A£Øg£©+3B£Øg£©ØT2C£Øg£©ÖŠ£¬ČōŅŌĪļÖŹA±ķŹ¾µÄøĆ·“Ó¦µÄ»Æѧ·“Ó¦ĖŁĀŹĪŖ0.2molL©1min©1 £¬ ŌņŅŌĪļÖŹB±ķŹ¾“Ė·“Ó¦µÄ»Æѧ·“Ó¦ĖŁĀŹĪŖmolL©1min©1 £®
£Ø2£©ŌŚ2LµÄĆܱÕČŻĘ÷ÖŠ£¬³äČė2mol N2ŗĶ3mol H2 £¬ ŌŚŅ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£¬3sŗó²āµĆN2ĪŖ1.9mol£¬ŌņŅŌH2µÄÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ £®
£Ø3£©½«10mol AŗĶ5mol B·ÅČėČŻ»żĪŖ10LµÄĆܱÕČŻĘ÷ÖŠ£¬Ä³ĪĀ¶ČĻĀ·¢Éś·“Ó¦£ŗ3A£Øg£©+B£Øg£©ØT2C£Øg£©£¬ŌŚ×ī³õ2sÄŚ£¬ĻūŗÄAµÄĘ½¾łĖŁĀŹĪŖ0.06molL©1s©1 £¬ ŌņŌŚ2sŹ±£¬ČŻĘ÷ÖŠ“ĖŹ±CµÄĪļÖŹµÄĮæÅضČĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹ¹ÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠ»ÆѧŠ”ŹµŃ飬ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ 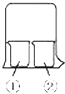
£Ø1£©Čō¢ŁÖŠ·ÅŅ»Ę¬ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½£¬¢Ś×°ÓŠÅØ°±Ė®£¬æɹŪ²ģµ½µÄŹµŃéĻÖĻóĪŖ
£Ø2£©Čō¢Ł×°ÓŠAlCl3ČÜŅŗ£¬¢Ś×°ÓŠÅØ°±Ė®£¬æɹŪ²ģµ½µÄŹµŃéĻÖĻóĪŖ
£Ø3£©Čō¢Ł×°ÓŠÅØĻõĖį£¬¢Ś×°ÓŠÅØ°±Ė®£¬æɹŪ²ģµ½µÄŹµŃéĻÖĻóĪŖ
£Ø4£©Čō¢Ł×°ÓŠÅØĻõĖį£¬¢Ś×°ÓŠNa2SO3ČÜŅŗ£¬ŹµŃ鏱ӊĪŽÉ«ĘųĢå²śÉś£¬øĆĘųĢåÖš½„±äĪŖŗģ×ŲÉ«£¬ÓĆ»Æѧ·½³ĢŹ½±ķŹ¾ĪŽÉ«ĘųĢå±äĪŖŗģ×ŲÉ«µÄŌŅņ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀ”¢³£Ń¹ĻĀ£¬ĻĀĮŠø÷×éĘųĢåÄܹ²“ęµÄŹĒ£Ø £©
A. NOŗĶO2 B. SO2ŗĶO2 C. H2SŗĶSO2 D. NH3ŗĶHCl
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķĪŖŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö£¬Ēė²ĪÕÕŌŖĖŲ¢Ł”«¢ąŌŚ±ķÖŠµÄĪ»ÖĆ£¬ÓĆŌŖĖŲ·ūŗÅ”¢Ąė×Ó·ūŗÅ»ņ»ÆѧŹ½»Ų“šĻĀĮŠĪŹĢā£ŗ 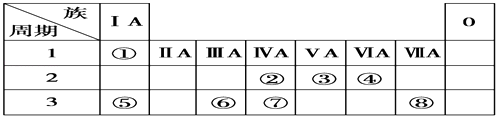
£Ø1£©¢Ü”¢¢Ž”¢¢ąµÄŌ×Ó°ė¾¶Óɓ󵽊”µÄĖ³ŠņŹĒ£ŗ£ØĒėÓĆ£¾”¢£¼±ķŹ¾£© £®
£Ø2£©¢Ś”¢¢Ū”¢¢ąµÄ×īøß¼Ūŗ¬ŃõĖįµÄĖįŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒ£ŗ £®
£Ø3£©ĒėŠ“³öÓÉ¢Ś”¢¢Ü”¢¢ßČżÖÖŌŖĖŲµÄĒā»ÆĪļĪČ¶ØŠŌÓÉČõµ½ĒæµÄĖ³ŠņŹĒ£ŗ £®
£Ø4£©¢Ż”¢¢ŽĮ½ÖÖŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļŌŚČÜŅŗÖŠĻą»„·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ£ŗ £®
£Ø5£©ÓɱķÖŠĮ½ÖÖŌŖĖŲµÄŌ×Ó°“1£ŗ1×é³ÉµÄŅ»ÖÖ³£¼ūŅŗĢ¬»ÆŗĻĪļµÄĻ”ČÜŅŗŅ×±» “߻Ʒֽā£¬æÉŹ¹ÓĆµÄ“ß»Æ¼ĮĪŖ£ØĢīŠņŗÅ£© £®
a£®KMnO4b£®MnO2c£®Na2SO3 £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ2LŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė2 mol XŗĶ1mol Y·¢Éś·“Ó¦£ŗ2X(g)+Y(g) ![]() 3Z(g) £¬·“Ó¦¹ż³Ģ³ÖŠųÉżøßĪĀ¶Č£¬²āµĆ»ģŗĻĢåĻµÖŠXµÄĢå»ż·ÖŹżÓėĪĀ¶ČµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĶʶĻÕżČ·µÄŹĒ( )
3Z(g) £¬·“Ó¦¹ż³Ģ³ÖŠųÉżøßĪĀ¶Č£¬²āµĆ»ģŗĻĢåĻµÖŠXµÄĢå»ż·ÖŹżÓėĪĀ¶ČµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĶʶĻÕżČ·µÄŹĒ( )
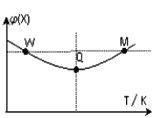
A. QµćŹ±£¬YµÄ×Ŗ»ÆĀŹ×ī“ó
B. WµćXµÄÕż·“Ó¦ĖŁĀŹµČÓŚMµćXµÄÕż·“Ó¦ĖŁĀŹ
C. ÉżøßĪĀ¶Č£¬Ę½ŗā³£ŹżŌö“ó
D. ĪĀ¶ČŅ»¶Ø£¬Ę½ŗāŹ±³äČėZ£¬“ļµ½ŠĀĘ½ŗāŹ±ZµÄĢå»ż·ÖŹż±ČŌĘ½ŗāŹ±“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬ÓĆ0.10mol”¤L-1NaOHČÜŅŗ·Ö±šµĪ¶Ø20.00mLÅØ¶Č¾łĪŖ0.10mol”¤L-1CH3COOHČÜŅŗŗĶHCNČÜŅŗĖłµĆµĪ¶ØĒśĻßČēĻĀĶ¼”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
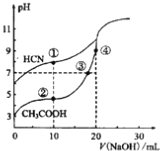
A. µć¢ŁŗĶµć¢ŚĖłŹ¾ČÜŅŗÖŠ£¬c(CH3COO-)-)
B. µć¢ŁŗĶµć¢ŚĖłŹ¾ČÜŅŗÖŠ£¬c(CH3COO-)-C(CN-)=c(HCN)-c(CH3COOH)
C. µć¢ÜĖłŹ¾ČÜŅŗŅŗÖŠ :c(Na+) >c(OH-)>c(CH3COO-) >c(H+)
D. µć¢ŚŗĶµć¢ŪĖłŹ¾ČÜŅŗÖŠ¶¼ÓŠ: c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠ²æ·Ö¶ĢÖÜĘŚŌŖĖŲµÄŠŌÖŹ”¢Ó¦ÓĆ»ņŌ×Ó½į¹¹ČēĻĀ±ķ£ŗ
ŌŖĖŲ±ąŗÅ | ŌŖĖŲŠŌÖŹ»ņŌ×Ó½į¹¹ |
T | M²ćµē×ÓŹżŹĒK²ćµē×ÓŹżµÄ3±¶ |
X | Ņ»ÖÖĶ¬Ī»ĖŲæɲā¶ØĪÄĪļÄź“ś |
Y | ³£ĪĀĻĀµ„ÖŹĪŖĖ«Ō×Ó·Ö×Ó£¬ĘäĒā»ÆĪļĖ®ČÜŅŗ³Ź¼īŠŌ |
Z | ŌŖĖŲ×īøßÕż¼ŪŹĒ+7¼Ū |
£Ø1£©ŌŖĖŲXæɲā¶ØĪÄĪļÄź“śµÄĶ¬Ī»ĖŲ·ūŗÅŹĒ £®
£Ø2£©ŌŖĖŲZŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖ £® Yµ„ÖŹµÄ½į¹¹Ź½ĪŖ £®
£Ø3£©ŌŖĖŲYÓėĒāŌŖĖŲŠĪ³ÉŅ»ÖÖĄė×ÓYH4+ £¬ ŹµŃéŹŅ¼ģŃéČÜŅŗÖŠŗ¬ÓŠÕāÖÖĄė×Ó·½·ØŹĒ£ŗ£Ø½öÓĆĄė×Ó·“Ó¦·½³ĢŹ½±ķŹ¾£©£®
£Ø4£©ŌŖĖŲZÓėŌŖĖŲTĻą±Č£¬·Ē½šŹōŠŌ½ĻĒæµÄŹĒ£ØÓĆŌŖĖŲ·ūŗűķŹ¾£©£¬ĻĀĮŠ±ķŹöÖŠÄÜÖ¤Ć÷ÕāŅ»ŹĀŹµµÄŹĒ £® a£®³£ĪĀĻĀZµÄµ„ÖŹŗĶTµÄµ„֏דĢ¬²»Ķ¬
b£®ZµÄĒā»ÆĪļ±ČTµÄĒā»ÆĪļĪȶØ
c£®Ņ»¶ØĢõ¼žĻĀZŗĶTµÄµ„ÖŹ¶¼ÄÜÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦
d£®ZµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌ±ČTµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌĒ森
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗĻ³É°±·“Ó¦£ŗN2£Øg£©+3H2£Øg£©2NH3£Øg£©”÷H=©92.4kJmol©1 £¬ ŌŚ·“Ó¦¹ż³ĢÖŠ£¬Õż·“Ó¦ĖŁĀŹµÄ±ä»ÆČēĶ¼£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £© 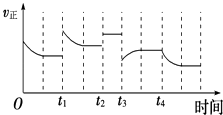
A.t1Ź±ÉżøßĮĖĪĀ¶Č
B.t2Ź±Ź¹ÓĆĮĖ“߻ƼĮ
C.t3Ź±Ōö“óĮĖŃ¹Ēæ
D.t4Ź±½µµĶĮĖĪĀ¶Č
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com