
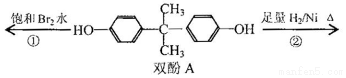
| A£® | Ė«·ÓAµÄ·Ö×ÓŹ½ŹĒC15H16O2 | |
| B£® | ·“Ó¦¢ŁÖŠ£¬1molĖ«·ÓA×ī¶ąĻūŗÄ2mol Br2 | |
| C£® | ·“Ó¦¢ŚµÄ²śĪļÖŠÖ»ÓŠŅ»ÖÖ¹ŁÄÜĶÅ | |
| D£® | Ė«·ÓAµÄŗĖ“Ź²ÕńĒāĘ×ĻŌŹ¾ĒāŌ×ÓŹżÖ®±ČŹĒ1£ŗ2£ŗ2£ŗ3 |
·ÖĪö ÓŠ»śĪļÖŠŗ¬ÓŠ·ÓōĒ»ł£¬ĒŅĮŚĪ»ŗ¬ÓŠĒāŌ×Ó£¬æÉ·¢ÉśČ”“ś”¢Ńõ»ÆŗĶĻŌÉ«·“Ó¦£¬ŗ¬ÓŠ±½»·£¬æÉ·¢Éś¼Ó³É·“Ó¦£¬½įŗĻÓŠ»śĪļµÄ½į¹¹½ā“šøĆĢā£®
½ā“š ½ā£ŗA£®Óɽį¹¹¼ņŹ½æÉÖŖĖ«·ÓAµÄ·Ö×ÓŹ½ĪŖC15H16O2£¬¹ŹAÕżČ·£»
B£®Ė«·ÓAÖŠ£¬2øö·ÓōĒ»łÓŠ4øöĮŚĪ»Hæɱ»Č”“ś£¬Ōņ1molĖ«·ÓA×ī¶ąĻūŗÄ4molBr2£¬¹ŹB“ķĪó£»
C£®¼Ó³É·“Ó¦ŗ󣬲śĪļµÄ¹ŁÄÜĶÅÖ»ÓŠ-OH£¬¹ŹCÕżČ·£»
D£®Į½øö¼×»łĻąĶ¬£¬Į½øö±½·Ó»łĻąĶ¬£¬øł¾Ż±½»·µÄ¶Ō³ĘæÉÖŖÓŠ4ÖÖ²»Ķ¬µÄH£¬HŌ×ÓŹżÖ®±ČŹĒ2£ŗ4£ŗ4£ŗ6=1£ŗ2£ŗ2£ŗ3£¬¹ŹDÕżČ·£®
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄ½į¹¹ŗĶŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦£¬ĢāÄæÄŃ¶Č²»“󣬱¾Ģā×¢Ņā°ŃĪÕÓŠ»śĪļ¹ŁÄÜĶŵĊŌÖŹ£¬ĪŖ½ā“šøĆĢāµÄ¹Ų¼ü£¬ŅדķµćĪŖD£¬×¢ŅāHŌ×ÓÖÖĄąµÄÅŠ¶Ļ£®


 ŗ®¼ŁĢģµŲÖŲĒģ³ö°ęÉēĻµĮŠ“š°ø
ŗ®¼ŁĢģµŲÖŲĒģ³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | OH-”¢H2O | B£® | NH3”¢NH4+ | C£® | H3O+”¢NH2- | D£® | HC1”¢H2S |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | m+n£¾p | B£® | Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ | ||
| C£® | AµÄ×Ŗ»ÆĀŹ¼õŠ” | D£® | CµÄĢå»ż·ÖŹżŌö¼Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| X | Y | |
| Z | ӊ | R |
| W |
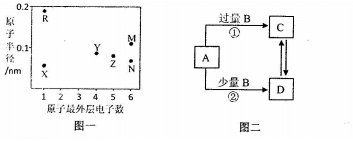
| A£® | Ō×Ó°ė¾¶“󊔹ŲĻµĪŖ£ŗR£¾Y£¾X | |
| B£® | XÓŠ¶ąÖÖĶ¬ĖŲŅģŠĪĢ壬¶ųY²»“ęŌŚĶ¬ĖŲŅģŠĪĢå | |
| C£® | øł¾ŻŌŖĖŲÖÜĘŚĀÉtæÉŅŌĶĘ²āWŌŖĖŲµÄµ„ÖŹ¾ßÓŠ°ėµ¼ĢåĢŲŠŌ£¬W2Y3¾ßÓŠŃõ»ÆŠŌŗĶ»¹ŌŠŌ | |
| D£® | Ēā»ÆĪļČŪ·Šµć£ŗH2R£¾H2Y |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
 £®
£® £¬ĖüÄÜÓėĖ«ŃõĖ®ŌŚĖįŠŌĢõ¼žĻĀ·“Ó¦£¬Éś³ÉĮ½ÖÖĪŽ¶¾ĘųĢ壬ĘäĄė×Ó·½³ĢŹ½ĪŖ2CN-+5H2O2+2H+ØTN2”ü+2CO2”ü+6H2O£®
£¬ĖüÄÜÓėĖ«ŃõĖ®ŌŚĖįŠŌĢõ¼žĻĀ·“Ó¦£¬Éś³ÉĮ½ÖÖĪŽ¶¾ĘųĢ壬ĘäĄė×Ó·½³ĢŹ½ĪŖ2CN-+5H2O2+2H+ØTN2”ü+2CO2”ü+6H2O£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
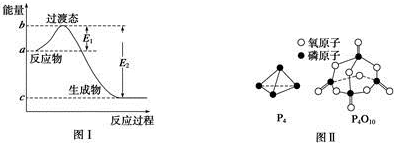
| »Æѧ¼ü | P-P | P-O | OØTO | PØTO |
| ¼üÄÜ/kJ•mol-1 | a | b | c | x |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1L 0.1mol/LµÄ°±Ė®ÖŠÓŠ0.1NAøöNH4+ | |
| B£® | 17 g H2O2ÖŠŗ¬ÓŠ8NAøöµē×Ó | |
| C£® | 7.8g Na2SŗĶ7.8g Na2O2Ėłŗ¬Ąė×ÓŹżĻąµČ£¬¾łĪŖ0.3 NA | |
| D£® | ±ź×¼×“æöĻĀ£¬22.4LNOÓė11.2LO2»ģŗĻŗóĘųĢåµÄ·Ö×ÓŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com