
【题目】对于反应2SiHCl3(g)= SiH2Cl2(g)+SiCl4(g) ΔH1=+48 kJ·mol-1,采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
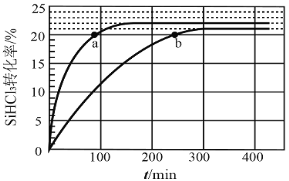
①343 K时反应的平衡转化率α=_________%。平衡常数K343 K=__________(保留2位小数)。
②在343 K下:要提高SiHCl3转化率,可采取的措施是__________,要缩短反应达到平衡的时间,可采取的措施有_____________。
③比较a、b处反应速率大小:υa______υb(填“大于”“小于”或“等于”)。反应速率υ=υ正υ逆=![]() ,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算a处
,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算a处![]() =________(保留1位小数)。
=________(保留1位小数)。
【答案】22 0.02 及时分离出产物 增大压强、使用催化剂或增大反应物的浓度等 大于 1.3
【解析】
①直接观察即可知343K时的平衡转化率,再根据转化率列出三段式,进而求出平衡常数K;
②影响平衡的因素有温度、压强及浓度等,可根据反应条件判断促进平衡正向移动,提高转化率的方法;要缩短反应达到平衡的时间,需要提高反应速率,而影响反应速率的因素主要有温度、浓度、压强及催化剂等。
③温度越高,反应速率越快,由图象观察a处和b处的温度大小比较即可;反应速率υ=υ正υ逆=![]() ,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数则a点时υ正=
,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数则a点时υ正=![]() ,υ逆=
,υ逆=![]() ,由平衡时正逆反应速率相等,可得出
,由平衡时正逆反应速率相等,可得出![]() ,再结合此温度下的平衡状态,计算出平衡常数K即可计算
,再结合此温度下的平衡状态,计算出平衡常数K即可计算![]() 。
。
温度越高,反应速率越快,图象中点a所在曲线为343K,由图示可知343K时反应![]() 的平衡转化率α=22%,设SiHCl3的起始浓度为cmol/L,则
的平衡转化率α=22%,设SiHCl3的起始浓度为cmol/L,则

平衡常数![]() ,
,
故答案为:22;0.02;
②由题目中前后反应气体体积不变,并且温度恒定,所以只能使用及时分离出产物的方法加大反应物的转化率;要缩短反应达到的时间,应增大反应速率,则在温度不变的条件下可采取的措施是:增大压强、使用催化剂或增大反应物的浓度等,故答案为:及时分离出产物;增大压强、使用催化剂或增大反应物的浓度等;
③由图象可知,a的反应温度高于b,温度高反应速率快,所以a点的反应速率比b高;a点时转化率为20%,设起始时SiHCl3的物质的量为nmol,此时
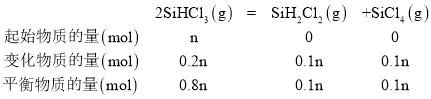
则:![]() ,
,![]() ;反应速率υ=υ正υ逆=
;反应速率υ=υ正υ逆=![]() ,k正、k逆分别为正、逆向反应速率常数,则a点时
,k正、k逆分别为正、逆向反应速率常数,则a点时![]() ,
,![]() ,由平衡时正逆反应速率相等,可得出
,由平衡时正逆反应速率相等,可得出![]() (平衡常数),则
(平衡常数),则![]() ,故答案为:大于;1.3。
,故答案为:大于;1.3。


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
【题目】常温下,向1L0.01mol·L-1一元酸HR溶液中逐渐通入氨气[常温下NH3·H2O电离平衡常数K=1.76×10-5],保持温度和溶液体积不变,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述不正确的是
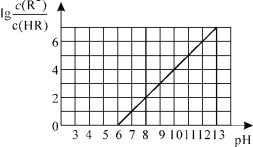
A.0.01mol·L-1HR溶液的pH约为4
B.随着氨气的通入,![]() 逐渐减小
逐渐减小
C.当溶液为碱性时,c(R-)>c(HR)
D.当通入0.01 mol NH3时,溶液中存在:c(R-)>c(NH4+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化学腐蚀实验。下列有关该实验的说法正确的是

A. 铁被氧化的电极反应式为Fe3e![]() Fe3+
Fe3+
B. 铁腐蚀过程中化学能全部转化为电能
C. 活性炭的存在会加速铁的腐蚀
D. 以水代替NaCl溶液,铁不能发生吸氧腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(16分)某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_______ ________。直到因加入一滴盐酸后,溶液由黄色变为橙色,并_______________为止。
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_______________
(A)酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
(B)滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
(C)酸式滴定管在滴定前有气泡,滴定后气泡消失
(D)读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:则起始读数为_________mL,终点读数为_____________mL;所用盐酸溶液的体积为______________ mL。
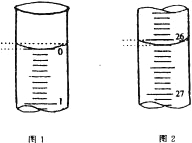
(4)某学生根据三次实验分别记录有关数据如下表:
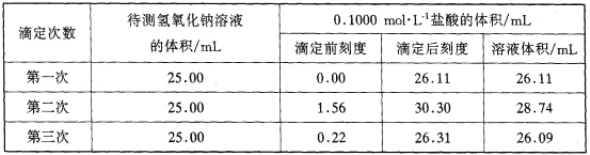
请用上述数据列式计算该氢氧化钠溶液的物质的量浓度 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒液流电池是一种新型的绿色环保储能系统,工作原理如图:
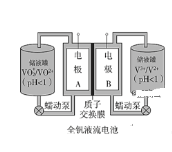
离子种类 | VO2+ | VO2+ | V3+ | V2+ |
颜色 | 黄色 | 蓝色 | 绿色 | 紫色 |
(1)全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是__________。
(2)当完成储能时,正极溶液的颜色是________
(3)质子交换膜的作用是____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1mol·L-1NaOH溶液滴定40mL0.1mol·L-1H2SO3溶液,所得滴定曲线如图所示(忽略混合时溶液体积的变化)。下列叙述正确的是( )
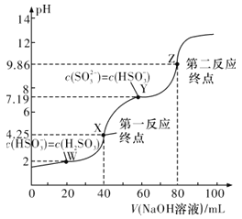
A.SO32-水解常数Kh的数量级为10-8
B.若滴定到第一反应终点,可用酚酞作指示剂
C.图中Z点对应的溶液中:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)
D.图中Y点对应的溶液中:3c(SO32-)=c(Na+)+c(H+)-c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝酸钙(mCaO·nAl2O3)是一系列由氧化钙和氧化铝在高温下烧结而成的无机化合物,被应用于水泥和灭火材料中,工业上用石灰石(主要成分为CaCO3和MgCO3)和铝土矿(主要成分是Al2O3、Fe2O3、SiO2等)制备铝酸钙的流程如图:
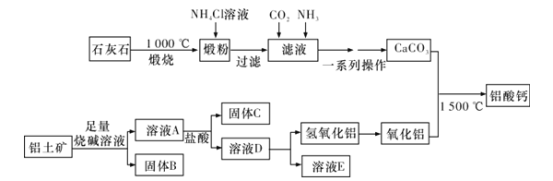
回答下列问题:
(1)固体B的主要成分是__(填化学式);一系列操作包括过滤、洗涤、干燥,洗涤过程应如何操作?__。
(2)向滤液中通入CO2和NH3的顺序为__,其理由是__。
(3)溶液D转化为Al(OH)3;离子方程式是__。
(4)常温下,用适量的NH4Cl溶液浸取煅粉后,若要保持滤液中c(Mg2+)小于5×10-6mol·L-1,则溶液的pH应大于__[已知:Mg(OH)2的K=5×10-12]。
(5)假设上述过程每一步均完全反应,最终得到的铝酸钙(3CaO·7Al2O3)的质量刚好等于原铝土矿的质量,该铝土矿中Al的质量分数为__(计算结果保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化过程的能量变化模拟计算结果如图所示,活化氧可以快速氧化二氧化硫。下列说法错误的是
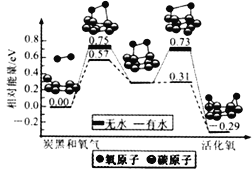
A. 氧分子的活化包括O-O键的断裂与C-O键的生成
B. 每活化一个氧分子放出0.29eV的能量
C. 水可使氧分子活化反应的活化能降低0.42eV
D. 炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型电池,以NaBH4(B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如下图所示。下列说法不正确的是

A. 每消耗3mol H2O2,转移6mol e-
B. 电池工作时Na+从b极区移向a极区
C. b极上的电极反应式为:H2O2 + 2e-= 2OH-
D. a极上的电极反应式为:BH4-+ 8OH--8e-=BO2-+6H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com