
����Ŀ������������һ�ְ�ɫ���壬������ˮ���������Ҵ�����ѧ����������������ơ�ijѧϰС������ڼ��Ի���������CaCl2��H2O2��Ӧ��ȡCaO2��8H2O��װ����ͼ��ʾ��

�ش��������⣺
��1��С��ͬѧ��������֪����ʵ������������Ϊ20%��H2O2��Һ��Ϊ���ˡ�����H2O2��Һ����������Ϊ30%����С��ͬѧ������H2O2��Һ����Լ20%��H2O2��Һ�Ĺ����У�ʹ�õIJ�������������������ͷ�ι��⣬����___��
��2������X����Ҫ���ó������⣬�����е�������___��
��3���ڱ�ˮԡ�н��е�ԭ����___��
��4��ʵ��ʱ����������ƿ������CaO2��8H2O���壬�ܷ�Ӧ�����ӷ���ʽΪ___��
��5����Ӧ���������ˡ�ϴ�ӡ����º�ɻ��CaO2��8H2O�������Լ��У�ϴ��CaO2��8H2O�����ѡ����____��
A����ˮ�Ҵ� B��Ũ���� C��Na2SO3��Һ D��CaCl2��Һ
��6����CaCl2ԭ���к���Fe3+���ʣ�Fe3+���ֽ�H2O2����ʹH2O2�����������Խ��͡���Ӧ�Ļ���Ϊ��
��Fe3+ +H2O2=Fe2++H++HOO��
��H2O2+X=Y +Z+W������ƽ��
��Fe2++��OH=Fe3++OH-
��H+ +OH-=H2O
�������������Ƶ�������еĻ�ѧ����ʽΪ___��
��7���������ƿ����ڳ�;�������磬�������˹������ƾ���____�����ʡ�
A.��ˮ������Ӧ���� B.���������������CO2����
C.����ˮ��������ǿ D.����ǿ�����ԣ���ɱ������
��8��������CaO2��8H2O������ȵ�150~160�棬��ȫ��ˮ��õ�����������Ʒ��
��С��ⶨ����������Ʒ��CaO2�Ĵ��ȵķ����ǣ�ȷ��ȡ0.4000g����������Ʒ��400�����ϼ�������ȫ�ֽ��CaO��O2(�����ʲ���������)���õ�33.60mL(�ѻ���Ϊ��״��)���塣
�����ù���������Ʒ��CaO2�Ĵ���Ϊ_____��
���𰸡��ձ�����Ͳ ��ֹ������ƿ����Һ�������� ��ֹ�¶ȹ���H2O2�ֽ⡢�����ھ������� Ca2++H2O2+2NH3+8H2O=CaO2��8H2O��+2NH4+ A HOO��+ H2O2=H2O + O2 +��OH ABD 54.00%
��������
����һ��������������Һ��Ҫ��������ֻ��Ҫ�ӳ���֪ʶ���
ͨ�백���Ӱ������ܽ���˼����
˫��ˮ�ڱ�ˮԡ�У���˫��ˮ�IJ��ȶ������⣬
����ԭ�ϺͲ�����д���ɰ�ˮ�������Ƶ����ӷ���ʽ��
�������ƾ�����������ʵó�ϴ�Ӱ�ˮ�������Ƶ��Լ���
�������ǰ���ϵ��˫��ˮ�ֽ�����ˮ��������֪ʶ�ó��м���T��Ӧ����ʽ��
���ù�ϵʽ���㴿�ȡ�
������Լ20%��H2O2��Һ�Ĺ����У�ʹ�õIJ�������������������ͷ�ιܡ��ձ�����Ͳ��
�ʴ�Ϊ���ձ�����Ͳ��
������X����Ҫ���ó������⣬��Ϊ������������ˮ����˻����з��������ã�
�ʴ�Ϊ����ֹ������ƿ����Һ����������
��˫��ˮ���ȷֽ⣬����ڱ�ˮԡ�н��е�ԭ���Ƿ�ֹ�¶ȹ���H2O2�ֽ⡢�����ھ���������
�ʴ�Ϊ����ֹ�¶ȹ���H2O2�ֽ⡢�����ھ�����������
��ʵ��ʱ����������ƿ������CaO2��8H2O���壬�ܷ�Ӧ�����ӷ���ʽΪCa2++H2O2+2NH3+ 8H2O =CaO2��8H2O��+2NH4+��
�ʴ�Ϊ��Ca2++H2O2+2NH3+8H2O=CaO2��8H2O��+2NH4+��
�ɹ���������һ�ְ�ɫ���壬������ˮ���������Ҵ������ϴ��CaO2��8H2O�����ʵ��Ϊ��ˮ�Ҵ���
�ʴ�Ϊ��A��
����CaCl2ԭ���к���Fe3+���ʣ�Fe3+���ֽ�H2O2��Ϊ������ˮ������ǰ����ϵ��˵�����в�����������ˮ������OH���仯ѧ����ʽΪ��HOO��+ H2O2=H2O + O2 +��OH��
�ʴ�Ϊ��HOO��+ H2O2=H2O + O2 +��OH��
�˹������ƿ����ڳ�;�������磬������Ҫ������˵���������ƾ�����ˮ������Ӧ��������������������Ķ�����̼�����ɱ�����ã�
�ʴ�Ϊ��ABD��
�̽�����CaO2��8H2O������ȵ�150~160������ȫ��ˮ��õ�����������Ʒ��
��С��ⶨ����������Ʒ��CaO2�Ĵ��ȵķ����ǣ�ȷ��ȡ0.4000g����������Ʒ��400�����ϼ�������ȫ�ֽ��CaO��O2(�����ʲ���������)���õ�33.60mL�����ʵ���Ϊ1.5��10-3 mol����
2CaO2 = 2CaO + O2
���ݹ�ϵ�ó�n(CaO2) = 3��10-3 mol��
![]() ��
��
�ʴ�Ϊ54.00%��


 ����ѵ��ϵ�д�
����ѵ��ϵ�д� ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ��������������ȷ����
A.31g���������P-P������NA
B.22.4LSO2����NA��SO2����
C.��״���£���������NO2��N2O4������ԭ�Ӹ������
D.1molCl2ͨ���ȵ�NaOH��Һ�У�������NaCl��NaClO3������ַ�Ӧ��ת�Ƶĵ�����ΪNA��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ȼ��ⱥ��ʳ��ˮ��ȡNaOH�Ĺ�������ʾ��ͼ���£�

������ͼ�����������գ�
��1���Ӻ�ˮ�л�ȡ���εķ�����___��
��2���������������У�����ȥ����ˮ�е�Ca2+��Mg2+��SO42-���ɽ��еIJ����У�
A. ����
B. �ӹ���BaCl2��Һ
C. ������ϡ����
D. �ӹ���NaOH��Һ
E. �ӹ���Na2CO3��Һ
����ȷ������˳����___(����ĸ)��
�ڲ���B��Ŀ����___
�۲���C��Ŀ����___
�ܲ���D�з�����Ӧ�����ӷ���ʽ��___
�ݴ˲����е�ϡ�����ܷ���ϡ�������?____(����������������)��������___��
��3������������������Һ����Ȼ����NaCl�ķ�����___���۲쵽��������___��
��4���������������У�ͨ������Ũ������ȴ�ᾧ��___�ķ�����ȥNaCl���÷�����ԭ������ͬ�¶���NaCl��NaOH���ܽ�Ȳ�ͬ���ڸò����¶��£��ܽ�Ƚϴ����___��
��5�����������п�ѭ��ʹ�õ�������______��(�ѧʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж����ʵ�������������ʵ����
A.����ˮ�����ڸ����µķ�Ӧ����ΪFe3O4��H2
B.��һС�ձ��зֱ����������ˮ��ú�ͣ�Ƭ�̺�������ձ��л����ؼ���һ�̶�����Ľ����ƣ����ܹ۲쵽����������ͼ

C.�ýྻ�IJ�˿պȡ����Һ�����ھƾ��ƻ��������գ��۲쵽����ʻ�ɫ�����������Һ��һ������Na+������K+
D.������ǯ��ס�����ھƾ����ϼ������ۻ�������ζ�����Һ̬������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧѧϰС���������װ�ã���Ũ������ľ̿�ķ�Ӧ����̽����
��֪��4HNO3![]() 4NO2����O2����2H2O
4NO2����O2����2H2O
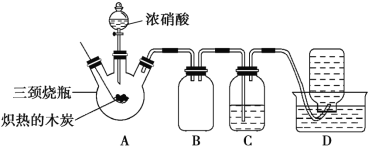
��ش��������⣺
��1�����װ�������Ժ�ȼ�ճ��е�ľ̿�ھƾ����ϼ���������״̬����������������ƿ�У�������ƿ�����μ�Ũ���ᣬ�ɹ۲쵽������ƿ���������ɫΪ____���������������Ҫ��ѧ��Ӧ����ʽ��_____��
��2��װ��C��ʢ������Ba(OH)2��Һ����Ӧһ��ʱ���ɹ۲쵽C�г��ְ�ɫ�������ð�ɫ����Ϊ____(�ѧʽ)�����е�Ba(OH)2��Һ___(������������������)��Ca(OH)2��Һ���棬������_____��
��3��װ��B��������___��
��4��װ��D���ռ�������ɫ���壬����ͬѧ��Ϊ��NO�����в���ͬѧ��Ϊ��O2��
�����жԸ�����ļ��鷽�����ʵ���__(�����)��
A�����ڹ۲켯��ƿ���������ɫ�仯
B������ʪ����ɫʯ����ֽ���뼯��ƿ�ڣ��۲���ֽ�Ƿ���
C���������ǵ�ľ�����뼯��ƿ�У��۲�ľ���Ƿ�ȼ
���������ƿ���ռ�������ɫ����������������������Դ��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A����̬������ȫȼ��ʱ������CO2�ͣ�H2O�����ʵ���֮��Ϊ1��1��A����Է�����С��30������ͼ��ʾ�ı仯�У��м����C��������һ��Ҳ�������Ƶ�Cu(OH)2������Ӧ����ש��ɫ������E����ζ��F�Ǹ߷��ӻ�����(��Ӧ����δд��)��
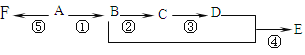
д�����и����仯�Ļ�ѧ����ʽ����Ӧ���͡�
��Ӧ��______��_______________
��Ӧ��______��________________
��Ӧ��______��___________________
��Ӧ��______��________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��װ��Ӧ����ͭ��Ũ���ᷴӦ��ȡ�������������ͭ���壬�ܴﵽʵ��Ŀ�ĵ���
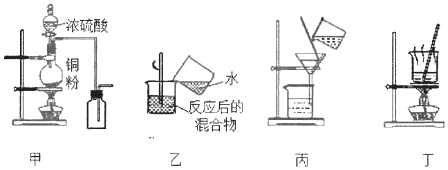
A. ��ͼ��װ����ȡ���ռ���������
B. ��ͼ��װ����Ӧ��Ļ�����м�ˮϡ��
C. ��ͼ��װ�ù��˳�ϡ�ͺ������еIJ�����
D. ��ͼ��װ�ý�����ͭ��Һ�����ᾧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ����
A.��FeBr2��Һ��ͨ������Cl2��2Br��+ Cl2 = Br2+ 2Cl��
B.��NH4Al(SO4)2��Һ�м������KOH��Һ��Al3+ + 4OH- = AlO2- + 2H2O
C.������������Һ���չ�ҵ�����е�NO2��2NO2 + 2OH- = NO3- + NO2- + H2O
D.�ö��Ե缫���AlCl3��Һ��2Cl- + 2H2O ![]() Cl2�� + H2�� + 2OH-
Cl2�� + H2�� + 2OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ100.0 mLNa2CO3��Na2SO4�Ļ����Һ���������BaCl2��Һ��õ�16.84g�������ù���ϡ���ᴦ�����������������6.99g,ͬʱ��Һ�������ݲ���������
��1��ԭ���Һ��Na2SO4�����ʵ���Ũ��Ϊ_____��
��2�������������ڱ�״���µ����Ϊ����__________����Ҫ��д��������̣�ֻд��������֣�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com