

 ;反应类型酯化反应会取代反应;
;反应类型酯化反应会取代反应;分析 (1)根据A的结构简式确定分子式,可知含有的官能团有羧基、醚键、氯原子;
(2)A中羧基甲醇发生酯化反应;
(3)氯原子水解得到酚羟基与HCl,酚羟基、HCl、羧基能与氢氧化钠反应;
(4)a.含有苯环的化合物为芳香族化合物;
b.均含有苯环,具有苯的性质,苯环可以发生加成反应、取代反应,羧基、酚羟基、氯原子也可以发生取代反应;
c.B苯环上的有5种H原子;
d.羧基能与碳酸氢钠反应,酚羟基不能与碳酸氢钠反应;
(5)亚硫酸比碳酸钠酸性强,亚硫酸氢根的酸性强于碳酸,在C溶液中通入少量SO2气体,反应得到无机物为亚硫酸钠;
(6)A的同分异构体E也含有“-OCH2COOH”,含有取代基还含有2个-Cl原子,2个-Cl原子有邻、间、对三种位置,移动-OCH2COOH确定同分异构体数目,C的水溶液中通入过量CO2生成的有机物F与B、D的分子式相同,结构不同,属于同分异构体.
解答 解:(1)根据A的结构简式,可知分子式为C8H6O3Cl2,含有的官能团有羧基、醚键、氯原子,
故答案为:C8H6O3Cl2;羧基、醚键、氯原子;
(2)A中羧基甲醇发生酯化反应,反应方程式为: ,属于取代反应,
,属于取代反应,
故答案为: ;酯化反应或取代反应;
;酯化反应或取代反应;
(3)氯原子水解得到酚羟基与HCl,酚羟基、HCl、羧基能与氢氧化钠反应,1molA水解得到2mol酚羟基、2molHCl,还含有1mol羧基,最多含有消耗5molNaOH,
故答案为:5;
(4)a.含有苯环的化合物为芳香族化合物,A、B、C都含有苯环,都属于芳香族化合物,故a正确;
b.均含有苯环,具有苯的性质,苯环可以发生加成反应、取代反应,羧基、酚羟基、氯原子也可以发生取代反应,故b正确;
c.B苯环上的有5种H原子,其一氯代物有5种,故c错误;
d.A含有羧基,能与碳酸氢钠反应生成二氧化碳,B含有酚羟基,不能与碳酸氢钠反应,故d错误,
故选:cd,
(5)亚硫酸比碳酸钠酸性强,亚硫酸氢根的酸性强于碳酸,在C溶液中通入少量SO2气体,反应得到无机物为亚硫酸钠,
故答案为:Na2SO3;
(6)A的同分异构体E也含有“-OCH2COOH”,含有取代基还含有2个-Cl原子,2个-Cl原子有邻、间、对三种位置,-OCH2COOH的位置分别有2种、3种、1种,除A外有5种,C的水溶液中通入过量CO2生成的有机物F与B、D的分子式相同,结构不同,属于同分异构体,
故答案为:5;同分异构体.
点评 本题考查有机物的结构与性质、限制条件同分异构体书写、官能团结构等,熟练掌握官能团的性质与转化.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
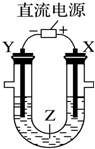
| A. | 氯碱工业中,X电极上反应式是4OH--4e-═2H2O+O2↑ | |
| B. | 电解精炼铜时,Z溶液中的铜离子浓度不变 | |
| C. | 在铁片上镀铜时,Y是纯铜 | |
| D. | 电解水制氢气时,Z可以是稀硫酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH+HCl═NaCl+H2O | B. | CuO+H2SO4═CuSO4+H2O | ||
| C. | Zn+2H+═Zn2++H2↑ | D. | CaO+H2O═Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 常温下,10mL pH均为2的HX、HY两种一元酸溶液,加水稀释过程中溶液的pH随溶液体积变化曲线如图所示.
常温下,10mL pH均为2的HX、HY两种一元酸溶液,加水稀释过程中溶液的pH随溶液体积变化曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
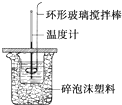 利用如图所示装置测定中和热的实验步骤如下:
利用如图所示装置测定中和热的实验步骤如下:| 温度 实验次数 | 超始温度t1℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | / |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的性质与用途: 磺胺类药物能抑制细菌合成核酸--治疗肺炎、脑膜炎、尿路感染、呼吸道感染 酸能与碱中和-----胃酸过多的病人服用含氢氧化钠的药物 | |
| B. | 保护环境: 控制“白色污染”--减少和控制使用所有塑料制品 防止水的污染--提倡使用无磷洗衣粉 | |
| C. | 基本安全常识: 饮用假酒中毒--由甲醇引起 食用假盐中毒--由亚硝酸钠引起 | |
| D. | 生活中的一些做法: 除去衣服上的油污--可用汽油洗涤 使煤燃烧更旺--可增大煤与空气接触面积 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第17.18列元素都是非金属元素 | |
| B. | 第14列元素形成的化合物种类最多 | |
| C. | 第3列元素种类最多 | |
| D. | 只有第2列元素的原子最外层有2个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com