
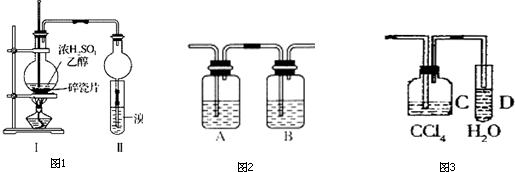
分析 (1)乙烯与溴发生加成反应生成1,2-二溴乙烷;
(2)浓H2SO4具有强氧化性,能将乙醇氧化成,根据SO2具有还原性,也能与溴水反应使溴水褪色,据此即可解答;
(3)1,2-二溴乙烷密度大于水,1,2-二溴乙烷在碱性条件下水解生成乙醇;
(4)在Ⅰ和Ⅱ之间增加图2装置,A装置是为了除去SO2和CO2,B装置是为了检验SO2是否除尽;
(5)若发生取代反应则会生成HBr,用硝酸银溶液检验会生成浅黄色沉淀.
解答 解:(1)乙烯使溴水褪色,乙烯与溴发生加成反应生成1,2-二溴乙烷,其反应的方程式为:CH2=CH2+Br2→CH2Br-CH2Br;
故答案为:CH2=CH2+Br2→CH2Br-CH2Br;
(2)浓H2SO4具有强氧化性,将乙醇氧化成碳,并且可以进一步反应,C+2H2SO4 (浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,SO2具有还原性,可以与Br2反应,SO2+Br2+2H2O=2HBr+H2SO4,所以bc正确,
故答案为:bc;
(3)溴水中的溴与乙烯发生加成反应生成 CH2BrCH2Br,1,2-二溴乙烷密度大于水,在试管底部,1,2-二溴乙烷在碱性条件下水解生成乙醇,其水解方程式为:CH2Br-CH2Br+2NaOH$→_{水}^{△}$ CH2OH-CH2OH+2NaBr;
故答案为:CH2Br-CH2Br+2NaOH$→_{水}^{△}$ CH2OH-CH2OH+2NaBr;
(4)在Ⅰ和Ⅱ之间增加图2装置,A装置是为了除去SO2和CO2,可用NaOH溶液吸收;B装置是为了检验SO2是否除尽,可用品红溶液,
故答案为:NaOH溶液;品红溶液;
(5)若发生取代反应则会生成HBr,可将产生的气体经净化后通入溴的四氯化碳溶液,再接入如图3装置,向 D中加入硝酸银溶液,若没有生成浅黄色沉淀说明没有HBr,即没有发生取代反应;
故答案为:硝酸银.
点评 本题考查了实验室制取1,2-二溴乙烷方法、乙烯的化学性质,题目难度中等,明确实验原理是解答本题的关键,根据浓硫酸、乙烯的性质来分析解答.


科目:高中化学 来源: 题型:解答题
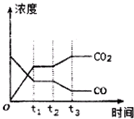 节能减排是当下环境保护的重点.
节能减排是当下环境保护的重点.| H2O | CO | CO2 | H2 | |
| n/mol | 0.20 | 0.20 | 0 | 0 |
| 容器编号 | c(CO)/mol•L-1 | c(O2))/mol•L-1 | c(CO2))/mol•L-1 | v(正)和v(逆)比较 |
| Ⅰ | 2.0×10-4 | 4.0×10-4 | 4.0×10-2 | v(正)=v(逆) |
| Ⅱ | 3.0×10-4 | 4.0×10-4 | 5.0×10-2 | v(正)>v(逆) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 操作 | 现象 | 结论 |
| 取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 | 溶液变(血)红色 | 存在Fe3+ |
| 取少量除尽Ag+后的溶液于试管中,加入1~2滴③或④(填序号)溶液,振荡 | 紫红色褪去或产生蓝色沉淀 | 存在Fe2+ |
| 实验编号 | 操 作 | 现 象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硝酸,振荡 | 黑色固体溶解,并有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若R(OH)n为强碱,则W(OH)n+1也为强碱 | |
| B. | 若最高氧化物的水化物HnXOm为强酸,则Y是活泼非金属元素 | |
| C. | 若Y的最低化合价为-2,则Z的最高正化合价为+6 | |
| D. | 若X的最高正化合价为+5,则五种元素都是非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
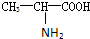 ),苯丙氨酸(
),苯丙氨酸(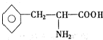 )
)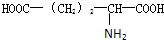 ),则该多肽中所含肽键的数目以及水解后得到的谷氨酸和苯丙氨酸的数目分别是( )
),则该多肽中所含肽键的数目以及水解后得到的谷氨酸和苯丙氨酸的数目分别是( )| A. | 10,4,3 | B. | 10,3,4 | C. | 9,4,3 | D. | 9,3,4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
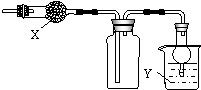 如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( )
如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( )| 选项 | X | 收集气体 | Y |
| A | 碱石灰 | 氯化氢 | 水 |
| B | 碱石灰 | 氨气 | 水 |
| C | 氯化钙 | 二氧化硫 | 氢氧化钠溶液 |
| D | 氯化钙 | 一氧化氮 | 氢氧化钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 亚硫酸钠溶液与双氧水混合:SO32-+2H2O2=SO42-+2H2O+O2↑ | |
| B. | NaClO溶液与FeCl2溶液混合:Fe2++2ClO-+2H2O=Fe(OH)2↓+2HClO | |
| C. | NH4HCO3溶液与足量NaOH溶液反应:NH4++OH-=NH3↑+H2O | |
| D. | 碳酸氢钙溶液中加入少量的氢氧化钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | I1/eV | I2/eV | I3/eV |
| 甲 | 5.7 | 47.4 | 71.8 |
| 乙 | 7.7 | 15.1 | 80.3 |
| 丙 | 13.0 | 23.9 | 40.0 |
| 丁 | 15.7 | 27.6 | 40.7 |
| A. | 甲的金属性比乙强 | B. | 乙的化合价为+1价 | ||
| C. | 丙一定为金属元素 | D. | 丁一定是金属元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com