
| A. | 1s电子云呈球形,表示电子绕原子核做圆周运动 | |
| B. | 电子云图中的小黑点密度大,说明该原子核外空间电子数目多 | |
| C. | 光谱分析可用于鉴定元素 | |
| D. | 3d3表示3d能级有3个轨道 |
分析 A.电子云表示表示电子在核外空间某处出现的机会;
B.小黑点的疏密表示电子出现机会的多少;
C.原子光谱是由原子中的电子在能量变化时所发射或吸收的一系列波长的光所组成的光谱,每一种原子的光谱都不同;
D.d3中的3表示d能级上的电子个数.
解答 解:A.电子云表示表示电子在核外空间某处出现的机会,不代表电子的运动轨迹,故A错误;
B.小黑点的疏密表示电子出现机会的多少,密则机会大,疏则机会小,故B错误;
C.原子光谱是由原子中的电子在能量变化时所发射或吸收的一系列波长的光所组成的光谱,每一种原子的光谱都不同,用原子光谱可以确定元素种类,故C正确;
D.3d3表示3d能级有3个电子,故D错误;
故选C.
点评 本题考查了电子云、原子轨道等知识点,易错选项是A,注意电子云中小黑点的疏密表示电子出现机会的多少,而不表示电子的数目,为易错点.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
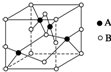 纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.回答下列问题:
纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2分子中,两个O之间形成2对共用电子对 | |
| B. | N2的电子式是N┇┇N | |
| C. | CO2和CS2都是直线型分子 | |
| D. | 白磷和甲烷都是正四面体型,键角都是109°28′ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室有一份混有碳酸钙杂质的碳酸钡样品.分离并提纯碳酸钡的实验步骤如下,请根据要求填空(如图为Ba(OH)2和Ca(OH)2的溶解度曲线):
实验室有一份混有碳酸钙杂质的碳酸钡样品.分离并提纯碳酸钡的实验步骤如下,请根据要求填空(如图为Ba(OH)2和Ca(OH)2的溶解度曲线):查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol任何气体的体积都约是22.4 L | |
| B. | 18 g NH4+含有电子数为10NA | |
| C. | NA个H2SO4分子的质量等于H3PO4的摩尔质量 | |
| D. | 标准状况下,相同体积的O2、HCl含有的分子数都为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com