
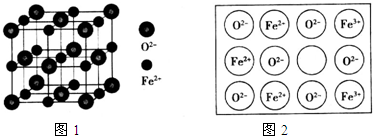
·ÖĪö £Ø1£©¾§Ģ唢·Ē¾§ĢåµÄ·½·ØŹĒXÉäĻßŃÜÉ䣻
£Ø2£©¹ģµĄÖŠµē×Ó“¦ÓŚČ«Āś”¢Č«æÕ”¢°ėĀśŹ±Ō×Ó×īĪČ¶Ø£»
£Ø3£©£ØSCN£©2·Ö×ÓÖŠ·Ö×Ó½į¹¹Ź½ĪŖN”ŌC-S-S-C”ŌN£¬ĆæøöSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹżŹĒ4ĒŅŗ¬ÓŠĮ½øö¹Āµē×Ó¶Ō£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪÅŠ¶ĻĮņŌ×ÓµÄŌӻƷ½Ź½£¬øĆ·Ö×ÓÖŠ¦Ņ¼üŗĶ¦Š¼üŹżÄæÖ®±ČĪŖ5£ŗ4£»ŗ¬ÓŠĒā¼üµÄĪļÖŹČŪ·Šµć½Ļøߣ»
£Ø4£©øĆ¾§°ūÖŠŃĒĢśĄė×ÓøöŹż=8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$=4£¬ŃõĄė×ÓøöŹż=1+12”Į$\frac{1}{4}$=4£¬
Éč¾§°ū±ß³¤ĪŖa cm£¬¾§°ūĢå»żĪŖa3cm3£¬ĆܶČĪŖb g•cm-3£¬°¢·ü¼ÓµĀĀŽ³£Źż=$\frac{4M}{¦ŃV}$£»
ijŃõ»ÆĪļѳʷ×é³ÉĪŖFe0.96O£¬»ÆŗĻĪļÖŠø÷ŌŖĖŲ»ÆŗĻ¼ŪµÄ“śŹżŗĶĪŖ0£¬øł¾ŻµēŗÉŹŲŗćÅŠ¶ĻøĆ¾§ĢåÖŠFe3+ÓėFe2+µÄĄė×ÓøöŹżÖ®±Č£®
½ā“š ½ā£ŗ£Ø1£©¾§Ģ唢·Ē¾§ĢåµÄ·½·ØŹĒXÉäĻßŃÜÉ䣬¹Ź“š°øĪŖ£ŗxÉäĻßŃÜÉ䣻
£Ø2£©¹ģµĄÖŠµē×Ó“¦ÓŚČ«Āś”¢Č«æÕ”¢°ėĀśŹ±Ō×Ó×īĪČ¶Ø£¬Cu+µÄ×īĶā²ćµē×ÓÅŲ¼Ź½ĪŖ3d10£¬¶ųCu2+µÄ×īĶā²ćµē×ÓÅŲ¼ĪŖ3d9£¬ŅņĪŖ×īĶā²ćµē×ÓÅŲ¼“ļµ½Č«ĀśŹ±ĪČ¶Ø£¬ĖłŅŌ¹ĢĢ¬Cu2OĪČ¶ØŠŌĒæÓŚCuO£¬¹Ź“š°øĪŖ£ŗCu+µÄ×īĶā²ćµē×ÓÅŲ¼Ź½ĪŖ3d10£¬¶ųCu2+µÄ×īĶā²ćµē×ÓÅŲ¼ĪŖ3d9£¬ŅņĪŖ×īĶā²ćµē×ÓÅŲ¼“ļµ½Č«ĀśŹ±ĪČ¶Ø£¬ĖłŅŌ¹ĢĢ¬Cu2OĪČ¶ØŠŌĒæÓŚCuO£»
£Ø3£©£ØSCN£©2·Ö×ÓÖŠ·Ö×Ó½į¹¹Ź½ĪŖN”ŌC-S-S-C”ŌN£¬ĆæøöSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹżŹĒ4ĒŅŗ¬ÓŠĮ½øö¹Āµē×Ó¶Ō£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪÖŖĮņŌ×ÓµÄŌӻƷ½Ź½ĪŖsp3£¬øĆ·Ö×ÓÖŠ¦Ņ¼üŗĶ¦Š¼üŹżÄæÖ®±ČĪŖ5£ŗ4£»ŗ¬ÓŠĒā¼üµÄĪļÖŹČŪ·Šµć½Ļøߣ¬ŅģĮņĒčĖį·Ö×Ó¼äÄÜŠĪ³ÉĒā¼ü¶ųĮņĒčĖį²»ÄÜŠĪ³ÉĒā¼ü£¬ĖłŅŌĮņĒčĖį£ØH-S-C”ŌN£©µÄ·ŠµćµĶÓŚŅģĮņĒčĖį£ØH-NØTCØTS£©µÄ·Šµć£¬
¹Ź“š°øĪŖ£ŗsp3£»5£ŗ4£»ŅģĮņĒčĖį·Ö×Ó¼äÄÜŠĪ³ÉĒā¼ü¶ųĮņĒčĖį²»ÄÜŠĪ³ÉĒā¼ü£»
£Ø4£©øĆ¾§°ūÖŠŃĒĢśĄė×ÓøöŹż=8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$=4£¬ŃõĄė×ÓøöŹż=1+12”Į$\frac{1}{4}$=4£¬
Éč¾§°ū±ß³¤ĪŖa cm£¬¾§°ūĢå»żĪŖa3cm3£¬ĆܶČĪŖb g•cm-3£¬°¢·ü¼ÓµĀĀŽ³£Źż=$\frac{4M}{¦ŃV}$=$\frac{4”Į72}{b”Į{a}^{3}}$/mol=$\frac{288}{{a}^{3}b}$/mol£»
ijŃõ»ÆĪļѳʷ×é³ÉĪŖFe0.96O£¬»ÆŗĻĪļÖŠø÷ŌŖĖŲ»ÆŗĻ¼ŪµÄ“śŹżŗĶĪŖ0£¬øł¾ŻµēŗÉŹŲŗćÅŠ¶ĻøĆ¾§ĢåÖŠFe3+ÓėFe2+µÄĄė×ÓøöŹżÖ®±Č£¬ÉčFe3+ÓėFe2+µÄøöŹż·Ö±šŹĒx”¢y£¬$\left\{\begin{array}{l}{x+y=0.96}\\{3x+2y=2}\end{array}\right.$£¬µĆ
$\left\{\begin{array}{l}{x=0.08}\\{y=0.88}\end{array}\right.$£¬ĖłŅŌx£ŗy=0.08£ŗ0.88=1£ŗ11£¬
¹Ź“š°øĪŖ£ŗ$\frac{288}{{a}^{3}b}$/mol£»1£ŗ11£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹ½į¹¹ŗĶŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬Éę¼°¾§°ū¼ĘĖć”¢Ō×ÓŌӻƷ½Ź½ÅŠ¶Ļ”¢Ēā¼ü”¢Ō×ÓŗĖĶāµē×ÓÅŲ¼µČÖŖŹ¶µć£¬ÖŖµĄĒā¼ü¶ŌĪļÖŹŠŌÖŹÓ°Ļģ”¢¹¹ŌģŌĄķ”¢¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪ”¢¾łĢƷصČÖŖŹ¶µć¼“æɽā“š£¬ÄѵćŹĒ£Ø4£©Ģā¾§°ū¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £¬Ė®ŃīĖįõ„EĪŖ×ĻĶāĪüŹÕ¼Į£¬æÉÓĆÓŚÅäÖĘ·ĄÉ¹ĖŖ£®EµÄŅ»ÖÖŗĻ³ÉĀ·ĻßČēĻĀ£ŗ
£¬Ė®ŃīĖįõ„EĪŖ×ĻĶāĪüŹÕ¼Į£¬æÉÓĆÓŚÅäÖĘ·ĄÉ¹ĖŖ£®EµÄŅ»ÖÖŗĻ³ÉĀ·ĻßČēĻĀ£ŗ
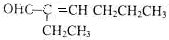 £»ČōÖ»ÄÜŅ»“ĪȔѳ£¬ĒėĢį³ö¼ģŃéCÖŠ2ÖÖ¹ŁÄÜĶŵļņŅŖ·½°ø£ŗÓĆŅų°±ČÜŅŗĻČ¼ģŃéČ©»ł£¬ŌŁ¼ÓĻ”ŃĪĖįŹ¹ČÜŅŗ³ŹĖįŠŌŗ󣬼ÓäåĖ®¼ģŃéĢ¼Ģ¼Ė«¼ü£»
£»ČōÖ»ÄÜŅ»“ĪȔѳ£¬ĒėĢį³ö¼ģŃéCÖŠ2ÖÖ¹ŁÄÜĶŵļņŅŖ·½°ø£ŗÓĆŅų°±ČÜŅŗĻČ¼ģŃéČ©»ł£¬ŌŁ¼ÓĻ”ŃĪĖįŹ¹ČÜŅŗ³ŹĖįŠŌŗ󣬼ÓäåĖ®¼ģŃéĢ¼Ģ¼Ė«¼ü£» ”¢HOCH2CH2C”ŌC-C”ŌC-COOH”¢
”¢HOCH2CH2C”ŌC-C”ŌC-COOH”¢ £»
£» £ŗ
£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 25”ꏱ£¬pH=1µÄ“×ĖįČÜŅŗÖŠŗ¬ÓŠH+µÄŹżÄæĪŖ0.1NA | |
| B£® | 100mL 18.4mol•L-1 µÄÅØĮņĖįÓė×ćĮæµÄĶ¼ÓČČ·“Ó¦ŗó£¬Éś³ÉSO2 ·Ö×ÓŹżĪŖ0.92NA | |
| C£® | ½«CO2 ĶعżNa2O2 £¬µ±¹ĢĢåÖŹĮæŌö¼Óa gŹ±£¬·“Ó¦ÖŠ×ŖŅʵĵē×ÓŹżĪŖa$\frac{{N}_{A}}{28}$ | |
| D£® | ±ź×¼×“æöĻĀ£¬11.2LÕż¶”ĶéĖłŗ¬¹«ÓƵē×Ó¶ŌŹżĪŖ7NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
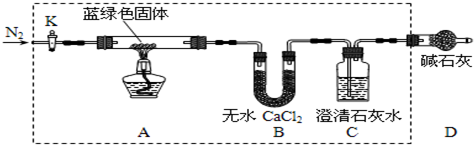
| Čܽā¶Č£ØS£©/g | ČܶȻż£ØKsp£© | Ħ¶ūÖŹĮæ£ØM£©/g•mol-1 | |||
| Ca£ØOH£©2 | Ba£ØOH£©2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9”Į10-9 | 2.6”Į10-9 | 100 | 197 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | x=y | B£® | x£¾y | C£® | x£¼y | D£® | ĪŽ·ØČ·¶Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 8ÖÖ | B£® | 10ÖÖ | C£® | 12ÖÖ | D£® | 13ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com