
| A. | 石油裂解可获得乙烯、丙烯和丁二烯 | |
| B. | 煤干馏可以得到甲烷、苯和氨等重要化工原料 | |
| C. | 天然植物油常温下一般呈液态,难溶于水,有固定的熔点、沸点 | |
| D. | 酚醛树脂、聚酯纤维(涤纶)都是由缩聚反应制得的高分子化合物 |
分析 A.裂解的目的是为了获得乙烯、丙烯、丁二烯、丁烯等;
B.煤干馏可以得到煤焦油,煤焦油中含有甲烷、苯和氨等重要化工原料;
C.混合物没有固定熔沸点;
D.缩聚反应是一类有机化学反应,是具有两个或两个以上官能团的单体,相互反应生成高分子化合物,同时产生有简单分子(如 H2O、HX、醇等)的化学反应;
解答 解:A.石油的裂解可获得乙烯、丙烯、丁二烯、丁烯等短链烯烃,故A正确;
B.因煤干馏可以得到煤焦油,煤焦油中含有甲烷、苯和氨等重要化工原料,可以通过分馏的方法进行分离,所以煤干馏可以得到甲烷、苯和氨等重要化工原料,故B正确;
C.天然植物油为混合物,不具有固定熔沸点,故C错误;
D.酚醛树脂是由苯酚和甲醛在催化剂条件下缩聚、经中和、水洗而制成的树脂,聚酯纤维是由饱和的二元酸与二元醇通过缩聚反应制得的一类线性高分子缩聚物,故D正确;
故选:C.
点评 本题考查石油的炼制、煤的干馏及有机物的结构与性质,明确石油裂解、煤干馏产物是解题关键,注意混合物不具有固定熔沸点,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 将SO2通入含HClO的溶液中生成H2SO4 HClO的酸性比H2SO4强 | |
| B. | 铝箔在酒精灯火焰上加热熔化但不滴落 铝箔表面氧化铝熔点高于铝 | |
| C. | SiO2可以和碱溶液及酸溶液反应 SiO2属于两性氧化物 | |
| D. | 将SO2通入溴水中,溴水褪色 SO2具有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某同学设计如图装置,研究非金属元素性质变化规律.
某同学设计如图装置,研究非金属元素性质变化规律.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
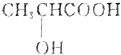 )有一对手性异构体,因为其分子中含有一个手性碳原子.
)有一对手性异构体,因为其分子中含有一个手性碳原子.| A. | 1句 | B. | 2句 | C. | 3句 | D. | 4句 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
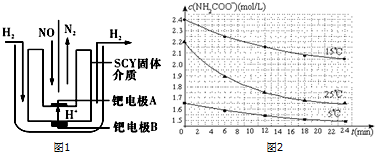
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
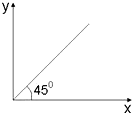
| A. | 第二周期的核电荷数和最高化合价之间的关系 | |
| B. | 烷烃中碳原子数(X)与氢原子数(Y)的关系 | |
| C. | 温度大于100℃时,CH4和C2H4的混合气体在氧气中充分燃烧,同温同压下燃烧前后参与反应的气体的体积之和(X)与生成物的气体体积之和(Y)的关系 | |
| D. | 燃烧一定质量C2H4与C3H6的混合气体,消耗O2的物质的量(Y)与C3H6的质量分数(X)的关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| KMnO4酸性溶液 的浓度/mol•L-1 | 溶液褪色所需时间 t/min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 12 |
| 0.001 | 6 | 7 | 7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com