
| A、原子半径:W>X>Z>Y |
| B、热稳定性:H2Y>HZ |
| C、离子半径:W2+>Y2- |
| D、碱性:XOH>W(OH)2 |
 ,然后根据元素周期律推断物质的性质,微粒半径大小比较.
,然后根据元素周期律推断物质的性质,微粒半径大小比较. ,
,

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
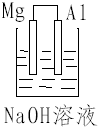 如图所示装置中:
如图所示装置中:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、冰的密度比液态水的密度小 |
| B、乙醇能跟水以任意比混溶 |
| C、NH3分子比PH3分子稳定 |
| D、在相同条件下,H2O的沸点比H2S的沸点高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素A、B组成的化合物可能是NH3 |
| B、一定条件下,元素C、D的最高价氧化物对应的水化物之间不能发生反应 |
| C、C、D、E的半径:C>D>E |
| D、化合物AE与CE具有相同类型的化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、E(3s)>E(2s)>E(1s) |
| B、E(3s)>E(3p)>E(3d) |
| C、E(4f)>E(4s)>E(5d) |
| D、E(5s)>E(4s)>E(4f) |
查看答案和解析>>
科目:高中化学 来源: 题型:
4 2 |
56 28 |
132 50 |
208 82 |
16 8 |
17 8 |
18 8 |
298 114 |
298 114 |
289 114 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com