

| A. | 1 mol亮菌甲素与溴水反应最多消耗3 mol Br2 | |
| B. | 分子中所有碳原子不可能共平面 | |
| C. | 1 mol亮菌甲素在一定条件下与NaOH溶液完全反应最多能消耗2 mol NaOH | |
| D. | 1 mol亮菌甲素在一定条件下可与6 mol H2发生加成反应 |
分析 苯和乙烯是平面结构,有机物中含酚-OH、醇-OH、C=C、-CO-、-COOC-,结合酚、烯烃、醇、酯的性质来解答.
解答 解:A.含酚-OH,与溴水在邻位发生取代反应,C=C与溴水发生加成反应,则1mol最多能和含3mol Br2的浓溴水反应,故A正确;
B.苯和乙烯是平面结构,取代苯环和乙烯中氢原子的碳原子,在同一平面内,所有碳原子可能共平面,故B错误;
C.酚-OH、-COOC-能与NaOH反应,且水解生成的酚-OH也反应,则1mol“亮菌甲素”能与含3molNaOH的溶液完全反应,故C错误;
D.苯环及C=C、-CO-能与氢气发生加成反应,1mol该物质最多能和5molH2发生加成反应,故D错误.
故选A.
点评 本题考查有机物的结构与性质,为高频考点,侧重考查学生的分析能力,注意把握有机物官能团与性质的关系来解答,熟悉酚、酯、烯烃的性质是解答的关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 四氧化三锰(Mn3O4)在电子工业有广泛应用.
四氧化三锰(Mn3O4)在电子工业有广泛应用.| 序号 | 反应 | △H(kJ•mol-1) | K | |
| 300°C | 800°C | |||
| Ⅰ | MnCO3(s)+$\frac{1}{2}$O2(g)?MnO2(s)+CO2(g) | a | 3.0×107 | 1.8×105 |
| Ⅱ | MnCO3(s)+$\frac{1}{4}$O2(g)?$\frac{1}{2}$Mn2O3(s)+CO2(g) | b | 1.7×103 | 2.4×105 |
| Ⅲ | MnCO3(s)+$\frac{1}{6}$O2(g)?$\frac{1}{3}$Mn3O4(s)+CO2(g) | c | 9.8 | 9.6×104 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 保持容器容积不变,向其中加入1 mol H2(g),再将平衡时反应速率一定加快 | |
| B. | 保持容器容积不变,向其中加入1 mol N2(N2不参加反应),反应速率一定加快 | |
| C. | 保持容器内气体压强不变,向其中加入1 mol N2(N2不参加反应),再次平衡时反应速率一定加快 | |
| D. | 保持容器内气体压强不变,向其中加入1 mol H2(g)和1 mol I2(g),再次平衡时反应速率一定加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
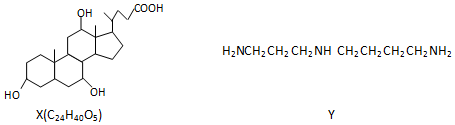
| A. | 1molX在浓硫酸作用下发生消去反应,最多生成3molH2O | |
| B. | 1molY发生类似酯化的反应,最多消耗2molX | |
| C. | X与足量HBr反应,所得有机物的分子式为C24H37O2Br3 | |
| D. | Y与癸烷的分子链均呈锯齿形,但Y的极性较强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素单质的熔点按F2、Cl2、Br2、I2的顺序依次减小 | |
| B. | 卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易 | |
| C. | 卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深 | |
| D. | 卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为△H=-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | CO(g)的燃烧热是283.0 kJ•mol-1,则CO2分解的热化学方程式为:2CO2(g)═2CO(g)+O2(g)△H=+283.0 kJ•mol-1 | |
| C. | 一定条件下,将0.5 mol N2(g)和1.5 mol H2(g)置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol-1 | |
| D. | 同温同压下,反应H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com