

科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
| 实验序号 | 1 | 2 | 3 | 4 | 5 |
| 硝酸溶液体积 | 100 mL | 200 mL | 300 mL | 400 mL | 500 mL |
| 剩余固体的质量 | 17.2 g | 8 .0g | 0 g | 0 g | 0 g |
| 气体体积 | 2.24 L | 4.48 L | 6.72 L | 7.84 L | 7.84 L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.5 mol/L | B.0.25 mol/L | C.5 mol/L | D.1 mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.(m-1.6)g | B.(m-2.4)g | C.(m-4.8)g | D.无法计算 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2.4g镁原子变成离子时,失去的电子数为0.3NA |
| B.常温常压下,28g氮气所含的原子数为2 NA |
| C.22.4L甲烷(CH4)所含的原子数为5NA |
| D.物质的量浓度为0.5mol / L的MgCl2溶液中,含有Cl—个数为1 NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在标准状况下,1mol水的体积是22.4L |
B.1mol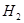 所占的体积一定是22.4L 所占的体积一定是22.4L |
C.1L0.5mol/L的 溶液中,含有 溶液中,含有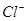 的个数为 的个数为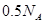 |
D.在标准状况下,总质量为28g的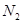 和CO的混合气体,其体积约为22.4L 和CO的混合气体,其体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.4mol·L-1 | B.6mol·L-1 | C.8mol·L-1 | D.10mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Mg和Al | B.Al和Fe |
| C.Fe和Zn | D.Zn和Cu |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com