
| A. | ①②③ | B. | ①③⑤ | C. | 全部 | D. | 都不是 |
分析 SO2具有酸性氧化物的通性、还原性、漂白性等性质,可与溴水、高锰酸钾等氧化剂发生氧化还原反应,以此解答该题.
解答 解:①SO2具有还原性,KMnO4酸性溶液具有氧化性,二者发生氧化还原反应而使紫红色KMnO4酸性溶液褪色,故正确;
②SO2具有酸性氧化物的通性,与碱发生反应生成盐和水而导致溶液PH减小,溶液 褪色或颜色变浅,故错误;
③SO2具有还原性,碘水具有氧化性,二者发生SO2+I2+2H2O═H2SO4+2HI,使碘水褪色,是由于SO2具有还原性,故正确;
④SO2具有漂白性,可使品红褪色,故错误;
⑤SO2具有还原性,Fe3+(aq)具有氧化性,二者发生氧化还原反应而使Fe3+(aq)褪色,故正确.
故选B.
点评 本题考查二氧化硫的性质,综合考查元素化合物知识,为高频考点,把握二氧化硫的漂白性、还原性为解答的关键,侧重基础知识的考查,题目难度不大.


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
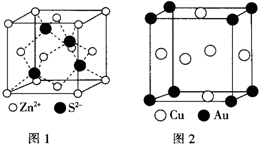
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 G在周期表的第七列 |
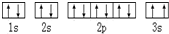 ,该同学所画的电子排布图违背了泡利不相容原理
,该同学所画的电子排布图违背了泡利不相容原理查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 被提纯的物质 | 除杂试剂 | 分离方法 | |
| A | SO2(乙炔) | 溴水 | 洗气 |
| B | 苯(溴) | KI溶液 | 分液 |
| C | 乙醇(乙酸) | 饱和Na2CO3溶液 | 蒸馏 |
| D | 乙烷(乙烯) | KMnO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | baecd | B. | edabc | C. | abdce | D. | ebadc |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
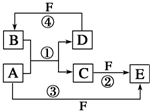 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).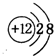 ,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2017届河南省南阳市高三上学期第三次月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数值,下列说法中错误的是
A.14g乙烯和甲烷混合气 体中的氢原子数一定大于2NA
体中的氢原子数一定大于2NA
B.2molN2与6molH2在一定条件下反应生成的NH3分子数一定大于2NA
C.56gFe溶于过量稀硝酸,电子转移数一定等于3NA
D.标准状况下,2.24LCH3Cl含有的共价键数一定等于0.4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com