
| A. | 一定量的碳酸氢钠溶液中加入足量澄清石灰水 HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 漂白粉的稀溶液中通入过量SO2气体 Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| C. | 已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O═2HClO+CO32- | |
| D. | Ba(OH)2溶液加入过量NaHSO4溶液中:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
分析 A.氢氧化钙足量,反应生成碳酸钙、氢氧化钠和水;
B.次氯酸根具有强的氧化性,能够氧化二氧化硫生成亚硫酸根离子;
C.酸性H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳生成HCO3-;
D.硫酸氢钠过量,二者反应生成硫酸钡、硫酸钠和水.
解答 解:A.定量的碳酸氢钠溶液中加入足量澄清石灰水,离子方程式:HCO3-+Ca2++OH-═CaCO3↓+H2O,故A正确;
B.漂白粉溶液中通入过量SO2的离子反应为Ca2++2ClO-+2H2O+2SO2=CaSO4↓+4H++2Cl-+SO42-,离子反应错误,故B错误;
C.向NaClO溶液中通入少量二氧化碳,生成HClO和HCO3-,离子方程式为ClO-+CO2+H2O═HClO+HCO3-,故错误;
D.Ba(OH)2溶液加入过量NaHSO4溶液中,离子方程式:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故D错误;
故选:A.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意反应物用量对反应的影响,注意次氯酸根离子的氧化性,题目难度不大.


科目:高中化学 来源: 题型:解答题
 苯甲酸苯酯是重要的有机合成中间体,工业上用二苯甲酮制备苯甲酸苯酯.
苯甲酸苯酯是重要的有机合成中间体,工业上用二苯甲酮制备苯甲酸苯酯.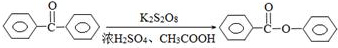
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以用铜丝或铁丝代替铂丝 | |
| B. | 用固体样品或配成的溶液进行实验,现象相同 | |
| C. | 每次实验前,铂丝要先用硫酸洗涤 | |
| D. | 焰色反应实验所用火焰,无论何种燃料均可 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | C5H12 | C. | C8H18 | D. | C9H20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1780 | B. | 1220 | C. | -1220 | D. | -1780 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
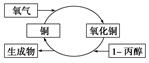
| A. | 1丙醇发生了还原反应 | |
| B. | 生成物可以发生银镜反应 | |
| C. | 反应中有红黑颜色交替变化的现象 | |
| D. | 2丙醇也能发生图示的催化氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上10月月考化学试卷(解析版) 题型:选择题
常温下Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16,将等体积的AgCl和AgI的饱和溶液 的清液混合,再向其中加入一定量的AgNO3固体,下列说法正确的是( )
的清液混合,再向其中加入一定量的AgNO3固体,下列说法正确的是( )
A.两溶液混合,AgCl和AgI都沉淀
B.若AgNO3足量,AgCl和AgI都可沉淀,但以AgCl为主
C.向AgI清液加入AgNO3,c(Ag+)增大,KSp(AgI)也增大
D.若 取0.1435克AgCl固体放入100mL水(忽略体积变化),c(Cl-)为0.01mol/L
取0.1435克AgCl固体放入100mL水(忽略体积变化),c(Cl-)为0.01mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com